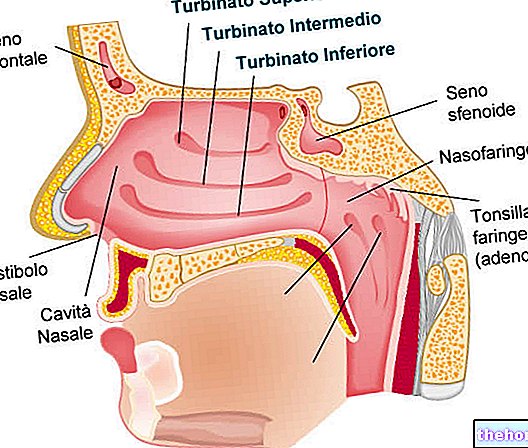
מרכיבים פעילים: אסטרדיול
טבלית נרתיק מצופה סרט Vagifem 25 מיקרוגרם
תוספות אריזה של Vagifem זמינות למידות האריזה:- טבלית נרתיק מצופה סרט Vagifem 25 מיקרוגרם
- Vagifem 10 מיקרוגרם טבליות נרתיק
אינדיקציות מדוע משתמשים ב- Vagifem? לשם מה זה?
VAGIFEM שייכת לקבוצת תרופות הנקראות אסטרוגנים.
הוא משמש לטיפול בדלקת הנרתיק אטרופית באסטרוגן.
הניסיון בנשים מעל גיל 65 מוגבל.
התוויות נגד כאשר אין להשתמש ב- Vagifem
אין להשתמש ב- "Vagifem":
- אם יש לך, היה לך או שאתה חשוד כחולה בסרטן השד
- אם היה לך או חשוד שיש לך גידול ממאיר שצמיחתו רגישה לאסטרוגן, למשל באנדומטריום (רירית הרחם)
- אם קיבלת או טופלת בעבר בקרישי דם בעורקים או בוורידים של הרגליים, או בריאות או בחלקים אחרים של הגוף (תסחיף)
- אם יש לך אנגינה (כאבים עזים בחזה) או אם עברת אוטם שריר הלב או שבץ
- אם יש לך פורפיריה (מחלה מטבולית תורשתית עקב שינוי בחילוף החומרים של פיגמנטים בדם)
- אם יש לך רגישות יתר לחומרים הפעילים או לאחד ממרכיבי התכשיר.
אמצעי זהירות לשימוש מה שאתה צריך לדעת לפני נטילת Vagifem
אם יש לך אחד מהמצבים הבאים, אנא הודע לרופא לפני תחילת הטיפול ב- "Vagifem':
- אם טרם חלפו 12 חודשים מאז המחזור החודשי
- אם יש לך או סבלת ממחלת כבד חמורה בעבר
- אם יש לך מחזור לא סדיר או דימום נרתיקי לאחרונה
- אם יש לך או הייתה לך "היפרפלזיה של רירית הרחם" (עיבוי רירית הרחם)
- אם יש לך אחת מהבעיות התורשתיות הנדירות הבאות: אי סבילות לגלקטוז, מחסור בלקטאז, תסמונת ספיגה של גלוקוז / גלקטוז.
שימו לב במיוחד בעת השימוש ב- "Vagifem":
לפני תחילת HRT, הרופא שלך ישאל אותך על ההיסטוריה הרפואית האישית והמשפחתית שלך. הרופא שלך עשוי לעבור בדיקת שד ו / או אגן (תחתון תחתון) ובדיקה גינקולוגית עבורך.
לאחר תחילת HRT, עדיין ייערכו בדיקות רפואיות קבועות (לפחות בשנה) כדי להעריך במדויק את הסיכונים והיתרונות של המשך הטיפול.
- לעבור בדיקת ממוגרפיה וציטולוגיה נרתיקית (בדיקת PAP) במרווחי זמן קבועים.
- בדוק באופן קבוע אם יש שינויים בשדיים כגון שקעים קטנים בעור, שינויים בפטמה או התקשות גלויה או ניכרת.
תנאים מסוימים יכולים להחמיר במהלך HRT. כך שאם יש לך, היו לך בעבר, או נמצאים בסיכון לאחד מהמצבים הבאים, הרופא שלך עשוי לבקש בדיקות תכופות יותר:
- שריר הרחם או אנדומטריוזיס (נוכחות של רירית הרחם במקומות חריגים) "
- היווצרות קרישי דם ברגליים או בריאות (ראה סעיף "קרישי דם")
- בן משפחה מדרגה ראשונה שיש לו או היה לו סרטן שד או גידול שצמיחתו רגישה לאסטרוגן (למשל סרטן הרחם או השחלות)
- יתר לחץ דם (לחץ דם גבוה)
- הפרעות בכבד
- סוכרת
- אבנים בכיס המרה
- מיגרנה או כאב ראש חמור
- זאבת מערכתית (מחלה אוטואימונית)
- אפילפסיה (מחלה המובילה להתקפים)
- אַסְתְמָה
- אוטוסקלרוזיס (מחלת אוזן תיכונה תורשתית)
- היפרטריגליצרידמיה (עלייה בטריגליצרידים בדם)
- אי ספיקת לב או כליות.
אם אתה מבחין בשינוי באחד מהתנאים שלעיל ואתה נוטל Vagifem, דווח לרופא שלך.
בשל הניהול המקומי של vagifem והריכוזים הנמוכים של אסטרדיול הכלולים בו, ההישנות או החמרה של התנאים הנ"ל, כמו גם הופעת התנאים שהוזכרו לעיל, פחות סבירה ממה שנצפה בטיפול מערכתי באסטרוגני.
עליך להפסיק את הטיפול ב- "Vagifem" באופן מיידי ולפנות לרופא שלך:
- אם העור שלך הופך צהוב (צהבת)
- אם אתה מבחין בעלייה משמעותית בלחץ הדם
- אם אתה מבחין בכאב ראש חמור פתאומי (כגון מיגרנה)
- במקרה של הריון.
השפעות על מערכת הלב וכלי הדם
מחלת לב
HRT אינו מומלץ לנשים הסובלות או שסבלו לאחרונה ממחלות לב. אם יש לך מחלת לב, ספר לרופא שלך על התחלת טיפול הורמונאלי. ל- HRT אין השפעה מונעת על מחלות לב.
מחקרים עם HRT המכילים אסטרוגנים מצומדים ומדרוקסיפוגסטרון אצטט כפרוגסטון הראו סיכון מוגבר למחלות לב במהלך השנה הראשונה לטיפול. עבור סוגים אחרים של HRT, הסיכון צפוי להיות דומה, אם כי עדיין לא הוכח.
תגיד לרופא שלך מיד אם אתה מרגיש כאבים בחזה המתפשטים לזרוע או לצוואר והפסיק לקחת את התרופה עד שהרופא שלך נותן לך אישור להמשיך. כאב זה יכול להיות סימפטום של מחלת לב.
שבץ
מחקרים שנעשו לאחרונה מצביעים על עלייה קטנה בסיכון לשבץ הקשור בשימוש ב- HRT. גורמים נוספים העלולים להגביר את הסיכון לשבץ כוללים:
- גיל
- לחץ דם גבוה
- עָשָׁן
- צריכת אלכוהול מופרזת
- פעימות לב לא סדירות.
ספר לרופא אם יש לך אחד מהגורמים הנ"ל או אם עברת שבץ בעבר לשקול להתחיל טיפול הורמונלי..
נתונים בהשוואה
עבור נשים שאינן משתמשות ב- HRT, נאמדו כ -3 מקרים של שבץ לכל 1,000 נשים בגילאי 50-59 וכ -11 לכל 1,000 נשים בגילאי 60-69 על פני 5 שנים.
לנשים המשתמשות ב- HRT, יש 4 שבץ לכל 1,000 נשים בגילאי 50-59 שנים ו -15 לכל 1,000 נשים בגילאי 60-69 שנים.
הודע לרופא מיד אם אתה מפתח כאבי ראש דמויי מיגרנה בלתי מוסברים עם או בלי הפרעות ראייה, והפסק ליטול את התרופה עד שהרופא יאשר לך להמשיך.
כאב ראש דמוי מיגרנה יכול להיות סימפטום מוקדם לשבץ.
טרומבוס
HRT עשוי להגביר את הסיכון להיווצרות קרישי דם בתוך הוורידים (המכונה גם פקקת ורידים עמוקים או DVT), במיוחד במהלך השנה הראשונה לטיפול. קרישי דם אלה אינם מסוכנים לרוב, אך אם הם מתנתקים. נסיעה לריאות, הם יכולים לגרום לכאבים בחזה, קשיי נשימה, קריסה ואפילו מוות. מצב זה מכונה תסחיף ריאתי או PE.
פקקת ורידים עמוקים ותסחיף ריאתי הם דוגמאות למצב המכונה טרומבואמבוליזם ורידי או VTE.
אתה נמצא בסיכון להיווצרות פקקת אם:
- אם אתם שמנים
- אם היו לך קרישי דם בעבר
- אם לבן משפחתך מדרגה ראשונה היו קרישי דם בעבר
- אם עברת הפלה אחת או יותר
- אם יש לך בעיות קרישה הדורשות טיפול בנוגדי קרישה (תרופות דמויי וורפרין)
- אם אתה צריך להיות משותק במשך זמן רב עקב ניתוח גדול, טראומה או מחלה
- אם יש לך מצב נדיר כגון זאבת מערכתית (SLE).
ספר לרופא אם יש לך אחד מהתנאים המפורטים לעיל כדי לשקול להתחיל טיפול הורמונלי.
נתונים בהשוואה
עבור נשים שאינן משתמשים ב- HRT, כ -3 מקרים של VTE לכל 1,000 נשים בגילאי 50-59 שנים וכ -8 ל -1,000 נשים בגילאי 60-69 שנים נאמדו על פני 5 שנים.
עבור נשים המשתמשות ב- HRT, מקרי VTE הופכים ל -7 לכל 1,000 נשים בגילאי 50-59 שנים ול -17 מקרים של VTE לכל 1,000 נשים בגילאי 60-69 שנים.
הודע לרופא מיד אם אתה נתקל בבצקת כואבת של הגפיים התחתונות (רגליים נפוחות), כאבים פתאומיים בחזה או קשיי נשימה, והפסק ליטול את התרופה עד שהרופא יאשר לך להמשיך. בעיות אלו עלולות להיות סימפטומים של טרומבואמבוליזם.
תגיד לרופא אם אתה צריך לעבור ניתוח.
HRT יופסק 4 עד 6 שבועות לפני הניתוח על מנת להפחית את הסיכון לקריש דם. הרופא שלך ייעץ לך לגבי חידוש טיפול הורמונאלי.
השפעות על הסיכון לסרטן
סרטן השד
נשים שחולות או חלו בסרטן השד לא צריכות ליטול HRT.
נטילת HRT מגבירה מעט את הסיכון לסרטן השד, כמו גם הופעה מאוחרת של גיל המעבר.
הסיכון לאישה לאחר גיל המעבר הנוטלת טיפול הורמונלי להפסקת טיפול בלבד באסטרוגן במשך 5 שנים שווה לזה של אישה בגיל זה שעדיין עוברת מחזור בזמן זה ואינה נוטלת טיפול הורמונלי. הסיכון לאישה הנוטלת אסטרוגן / פרוגסטוגן HRT משולב גבוה יותר מאשר לנשים הנוטלות אסטרוגן לבד (אך לשילוב האסטרוגן-פרוגסטגן יש יתרונות לאנדומטריום, ראה סעיף "סרטן רירית הרחם").
לכל HRT, הסיכון הנוסף לסרטן השד מתגלה תוך שנים ספורות מתחילת הטיפול ועולה עם משך השימוש, אך חוזר לקו הבסיס תוך כ -5 שנים לאחר הפסקת הטיפול.
הסיכון לסרטן השד מגביר גם:
- אם יש לך קרוב משפחה מדרגה ראשונה (אמא, אחות או סבתא) שחלה בסרטן השד
- אם אתם שמנים.
נתונים בהשוואה
בקרב נשים בשנות ה -50 לחייהן שאינן משתמשות ב- HRT, מאובחנות כ -32 סרטן שד לכל 1,000 נשים בתקופה עד גיל 65. בקרב נשים המתחילות ב- HRT רק לאסטרוגן בגיל 50 ולוקחות אותו במשך 5 שנים, יהיו 33-34 לכל 1,000 נשים שאובחנו כסובלות מסרטן השד (1-2 מקרים נוספים).
אם הצריכה נמשכת 10 שנים, סרטן השד המאובחן הופך ל -37 לכל 1,000 נשים (5 מקרים נוספים).
לנשים המתחילות טיפול משולב ב- HR עם אסטרוגן-פרוגסטגן בגיל 50 ונוטלות אותו במשך 5 שנים, יהיו 38 סרטן שד מאובחנים לכל 1,000 נשים (6 מקרים נוספים).
אם הצריכה נמשכת 10 שנים, סרטן השד המאובחן הופך ל -51 לכל 1,000 נשים (19 מקרים נוספים).
פנה לרופא בהקדם האפשרי אם אתה חווה שינויים בחזה כגון שקעים קטנים בעור, שינויים בפטמה או התקשות נראית או מורגשת.
סרטן רירית הרחם (סרטן רירית הרחם)
נטילת HRT רק לאסטרוגן לאורך זמן עשויה להגביר את הסיכון לחלות בסרטן רירית הרחם.
נטילת פרוגסטוגן בנוסף לאסטרוגן מפחיתה את הסיכון הנוסף.
מינון האסטרדיול ב- Vagifem נמוך והטיפול מקומי. אצל חלק מהחולים עלולה להתרחש ספיגה מערכתית צנועה.
אם הרחם עדיין קיים, הרופא שלך ישקול האם יש צורך לרשום פרוגסטוג הקשור לאסטרוגן או משולב HRT של אסטרוגן-פרוגסטגן.
אם הרחם הוסר (עם כריתת רחם), הרופא שלך ידון איתך בכדאי לקחת רק את האסטרוגן ללא הפרוגסטוג המשויך.
אם הרחם הוסר חלקית עקב אנדומטריוזיס, כל שאר שאריות רירית הרחם עלולות להיות בסיכון. לאחר מכן הרופא שלך ידון איתך בנכונות נטילת אסטרוגן-פרוגסטגן HRT.
נתונים בהשוואה
בקרב נשים שאין לה רחם שאינן מטופלות ב- HRT, מאובחנים כ -5 מקרים של סרטן רירית הרחם לכל 1,000 נשים בגילאי 50-65.
בקרב נשים המשתמשות ב- HRT לאסטרוגן בלבד, המספר גדל פי 2 עד פי 12 כתלות במינון ומשך הטיפול.
הוספת פרוגסטוגן ל- HRT לאסטרוגן מפחיתה באופן משמעותי את הסיכון לסרטן רירית הרחם.
הופעת דימום או כתמים בין הווסת (הפרשות בין -וסתיות קטנות) במיוחד במהלך קורסי הטיפול הראשונים לא אמורה להדאיג אותך.
פנה לרופא אם דימום פורץ או כתמים ממשיכים להתרחש לאחר חודשי הטיפול הראשונים, מופיע לאחר מספר חודשי טיפול או ממשיך לאחר הפסקת הטיפול: תסמינים אלה יכולים להצביע על עיבוי של רירית הרחם.
סרטן שחלות
סרטן השחלות (סרטן השחלות) הוא מצב נדיר מאוד אך חמור. האבחנה קשה מכיוון שלעיתים קרובות לא קיימים תסמינים ברורים.
כמה מחקרים הראו כי נטילת HRT בלבד לאסטרוגן במשך יותר מחמש שנים מעלה את הסיכון לסרטן השחלות. לא ידוע אם סוגים אחרים של HRT עשויים להגביר את הסיכון באופן דומה.
דמנציה
ל- HRT אין השפעה מונעת על אובדן הזיכרון. מחקר שנערך בקרב נשים שהתחילו טיפול משולב ב- HRT אסטרוגן-פרוגסטגן לאחר גיל 65, הצביע על סיכון מוגבר לדמנציה.
תנאים אחרים
נשים הסובלות מהיפרטריגליצרידמיה הנוטלות HRT עלולות לחוות עלייה מופרזת בטריגליצרידים בדם אשר עלולות להוביל לדלקת בלבלב.
אם אתה לוקח טיפול החלפת בלוטת התריס (המבוסס על תירוקסין) הזהיר את הרופא שלך, שעשוי לדרוש בדיקות תכופות יותר של תפקוד בלוטת התריס.
HRT יכול להשפיע על התוצאות של כמה בדיקות דם או שתן. תגיד לרופא שאתה לוקח Vagifem אם הוא מבקש ממך לבצע בדיקות הורמונליות.
אינטראקציות אילו תרופות או מזונות עשויים לשנות את ההשפעה של Vagifem
ספר לרופא אם אתה נוטל או נטלת לאחרונה תרופות אחרות - אפילו תרופות שאינן נקבעות.
עם זאת, מכיוון ש- Vagifem ניתנת באופן מקומי ומכילה מינון נמוך של אסטרדיול, לא נחשב לא סביר כי יחולו אינטראקציות עם מוצרי תרופות אחרים.
אזהרות חשוב לדעת כי:
הֵרָיוֹן
"Vagifem" אינו מסומן בהריון.
אם אתה חושד בהריון, אל תיקח את התרופה. אם הינך בהריון, השעה מ
זמן האכלה
אם את מניקה, אל תיקח את התרופה.
השפעה על כושר הנהיגה והשימוש במכונות
אף אחד.
מידע חשוב על חלק ממרכיבי "ואגיפם"
Vagifem מכיל לקטוז. אם הרופא שלך איבחן אותך כ"אי סבילות לכמה סוכרים, פנה אליו לפני נטילת התרופה ".
מינון ושיטת השימוש אופן השימוש ב- Vagifem: מינון
השתמש תמיד ב- Vagifem בדיוק כפי שהרופא שלך אמר לך. אם יש לך ספק עליך להתייעץ עם הרופא שלך.
מִנוּן
Vagifem ניתנת תוך ורידית באמצעות האפליקטור המיוחד. מנה ראשונית: טבליה אחת בנרתיק ביום למשך שבועיים.
מינון תחזוקה: טבליה אחת בנרתיק פעמיים בשבוע.
ניתן להתחיל את הטיפול בכל יום.
אם מחמיצים מנה, יש ליטול אותה ברגע שאתה זוכר. הימנע מנטילת מנה כפולה.
לתחילת הטיפול להמשך הסימפטומים לאחר גיל המעבר, יש להשתמש במינון הנמוך ביותר האפקטיבי למשך הזמן הקצר ביותר האפשרי.
ניתן להשתמש ב- Vagifem בשתי נשים עם רחם שלם ונשים עם כריתת רחם.
ספיגה מינימלית עשויה להתרחש במהלך הטיפול, במיוחד בשבועיים הראשונים, אך מכיוון שרמות הפלזמה של אסטרדיול לאחר השבועיים הראשונים בדרך כלל אינן עולות על אלה שנמצאו בתקופה שלאחר גיל המעבר, הוספה של פרוגסטוגן אינה מומלצת.
יש להמשיך בטיפול רק כל עוד התועלת המתקבלת בהקלה על תסמינים חמורים עולה על הסיכון.
מִנהָל
- הוציאו שלפוחית אחת ופתחו אותה בקצותיה כפי שמוצג. (איור)
- הכנס בזהירות את המוליך לנרתיק עד להתנגדות. (איור)
- כדי לשחרר את הטאבלט, לחץ על הכפתור בזהירות עד שתשמע נקישה. הלוח מוגן אפוא באופן מיידי על ידי דופן הנרתיק. הוא לא ייפול אם הוא עומד או הולך. (אִיוּר)
- הוציאו את המוליך וזרקו אותו.
שכחת בקשה
אל תיקח מנות כפולות כדי להחליף את מה שנשכח. אם שכחת ליטול לוח נרתיק, קח אחת ברגע שאתה זוכר.
חסר טבליה אחת או יותר של Vagifem עשוי להגדיל את הסבירות לדימום פורץ דרך או כתמים.
מנת יתר מה לעשות אם נטלת יותר מדי Vagifem
תסמינים של מנת יתר עשויים לכלול: בחילה, הקאות.
תסמינים אלה נעלמים עם הפסקת הטיפול או הפחתת המינון.
במקרה של צריכת מינון מוגזם של התרופה בשוגג, הודע לרופא מיד או פנה לבית החולים הקרוב.
אם יש לך ספקות בנוגע לשימוש ב- VAGIFEM, אנא צור קשר עם הרופא או הרוקח שלך.
תופעות לוואי מהן תופעות הלוואי של Vagifem
כמו כל התרופות, ל- "Vagifem" יכולות להיות תופעות לוואי שבדרך כלל נעלמות לאחר חודשי הטיפול הראשונים אותן ניתן לחלק כדלקמן:
יותר מ -640 מטופלים טופלו ב- Vagifem בניסויים קליניים שונים, כולל מעל 200 חולים שטופלו במשך 28-64 שבועות. אירועי לוואי הקשורים בהחלט למתן אסטרוגנים שהתרחשו בשכיחות גבוהה בקבוצת הטיפול בהשוואה לחולים שאינם מטופלים (פלסבו), מסווגים כ"נפוצים (> 1/100;
שיעור הגילוי הספונטני של תופעות לוואי הקשורות ל- Vagifem הוא כ -1 מקרה לכל 10,000 שנות חולה. אירועים שליליים שבהם לא נמצאה תדירות מוגברת בניסויים קליניים, אך אשר דווחו באופן ספונטני ואשר יש לשקול על דעתם פה אחד כי הם קשורים אולי לטיפול ב- Vagifem מסווגים אפוא כ"נדירים מאוד (
ניסיון שלאחר השיווק אינו כפוף לדיווח, במיוחד לתגובות שליליות קלות וכבר מוכרות.לכן יש לפרש את התדרים המוצגים לאור האמור לעיל.
תופעות הלוואי השליליות המדווחות ביותר הן: דימום והפרעות בנרתיק. תופעות לוואי הקשורות לטיפול באסטרוגן כגון כאבי שד, בצקת היקפית ודימום לאחר גיל המעבר מופיעים ככל הנראה רק בתחילת הטיפול ב- Vagifem.
תגובות הלוואי הבאות דווחו בשיתוף עם טיפול באסטרוגן:
- אוטם בשריר הלב ומחלות לב
- כולליתיאזיס
- הפרעות עור ורקמות תת עוריות: קלואזמה, אריתמה רב -פורמטית, אריתמה נודוסום, פורפורת כלי הדם, גירוד
- קנדידה נרתיקית
- סיכון לפתח סרטן רירית הרחם (ראה סעיף 4.4)
- היפרפלזיה רירית הרחם או שריר הרחם מוגדל *
- טרומבואמבוליזם ורידי
- נדודי שינה
- אֶפִּילֶפּסִיָה
- הפרעות בחשק המיני
- החמרה באסתמה
- דמנציה אפשרית (ראה סעיף 4.4).
* בנשים שאינן כריתות רחם
בדרך כלל תופעות לוואי אינן שכיחות ואינן נמשכות זמן רב.
יהיה עליך להפסיק לקחת "Vagifem" ולפנות לרופא שלך:
- אם מתרחשת היווצרות פקקת (ראה סעיף "פקקת")
- אם יש לך פתאום ראייה לקויה, כאב ראש חמור או מיגרנה (ראה סעיף "שבץ מוחי")
- אם אתה חווה כאבים פתאומיים בחזה המתפשטים לזרוע או לצוואר (ראה סעיף "מחלות לב")
- אם העור שלך הופך צהוב (צהבת)
- במקרה של הריון.
אם אחת מתופעות הלוואי הופכת חמורה, או אם אתה מבחין בתופעות לוואי שאינן מופיעות בעלון זה, דווח לרופא או לרוקח.
תפוגה ושמירה
יש להרחיק את Vagifem מהישג ידם של ילדים.
אין להשתמש ב- Vagifem לאחר תאריך התפוגה המופיע על התווית
תאריך התפוגה מתייחס ליום האחרון בחודש.
תאריך התפוגה המצוין מתייחס למוצר באריזה שלמה, מאוחסן כהלכה.
אין לאחסן מעל 25 ° C. אין לאחסן במקרר. שמור את המיכל בקרטון החיצוני.
אסור להשליך תרופות דרך שפכים או פסולת ביתית. שאל את הרוקח כיצד עליך לזרוק תרופות שאינך משתמש בהן יותר. הדבר יעזור להגן על הסביבה.
מה מכיל Vagifem
טבלית נרתיק אחת מצופה בסרט מכילה:
מרכיבים פעילים: אסטרדיול 25 מיקרוגרם (בתור האסטרדיול המהיהידרט)
חומרים עזר: היפרומלוז, לקטוז מונוהידראט, עמילן תירס, סטארט מגנזיום
ציפוי סרט: היפרומלוז ומקרוגול 6000.
איך נראית Vagifem ותכולת האריזה
Vagifem מגיע בצורה של טבליות נרתיק מצופות סרט.
כל טבלט מונח במוליך חד פעמי.
האפליקטורים ארוזים בשלפוחיות.
כל חבילה מכילה 15 מוליכים. הלוחות חקוקים ב- NOVO 279.
עלון המקור: AIFA (סוכנות התרופות האיטלקית). תוכן שפורסם בינואר 2016. ייתכן שהמידע הנוכחי אינו מעודכן.
כדי לקבל גישה לגרסה העדכנית ביותר, מומלץ לגשת לאתר AIFA (סוכנות התרופות האיטלקית). כתב ויתור ומידע שימושי.
01.0 שם התרופה
VAGIFEM
02.0 הרכב איכותי וכמותי
כל טבלית נרתיק מצופה בסרט מכילה: מרכיב פעיל. אסטרדיול: 25 מק"ג (כאסטרדיול המהיהידרט) של
לרשימת החומרים המלאים ראו סעיף 6.1.
03.0 טופס פרמצבטי
טבליות נרתיק מצופות סרט.
טבליות לבנות, קמורות, מצופות בסרט, חרותות NOVO 279. קוטר: 6 מ"מ.
Vagifem נמצא בטבליות הידרופיליות, עם מטריצה שמקורן בתאית אשר נוזל במגע עם לחות, ומשחרר 17β-אסטרדיול.
04.0 מידע קליני
04.1 אינדיקציות טיפוליות
Vagifem מיועדת לטיפול בדלקת הנרתיק אטרופית באסטרוגן.
הניסיון בטיפול בנשים מעל גיל 65 מוגבל.
04.2 מינון ושיטת הניהול
Vagifem ניתנת תוך ורידית באמצעות האפליקטור המיוחד. מנה ראשונית: טבליה נרתיקית אחת למשך שבועיים. מנה תחזוקה: טבליה אחת בנרתיק פעמיים בשבוע.
ניתן להתחיל את הטיפול בכל יום. במקרה של החמצת מנה, עדיף ליטול אותה ברגע שאתה זוכר, עדיף להימנע מנטילת מנה כפולה. לצורך התחלה והמשך הטיפול בסימפטומים לאחר גיל המעבר יש להשתמש במינון הנמוך ביותר האפקטיבי למשך הזמן הקצר ביותר האפשרי (ראו גם סעיף 4.4) ניתן להשתמש ב- Vagifem הן בנשים עם רחם שלם והן בנשים שעברו כריתת רחם. במהלך הטיפול מינימלי. ספיגה עלולה להתרחש, במיוחד בשבועיים הראשונים, אך מכיוון שרמות הפלזמה של אסטרדיול לאחר השבועיים הראשונים בדרך כלל אינן עולות על אלה שנמצאו בתקופה שלאחר גיל המעבר, לא מומלץ להוסיף פרוגסטוגן. יש להמשיך בטיפול רק כל עוד התועלת המתקבלת בהקלה על תסמינים חמורים עולה על הסיכון.
מִנהָל
פתח את השלפוחית מצד הכפתור.
הכנס את המוליך לנרתיק עד למצב ההתנגדות (8-10 ס"מ).
שחרר את הטאבלט על ידי לחיצה על הכפתור.
הסר את המוליך וזרק אותו.
04.3 התוויות נגד
- סרטן השד הנוכחי, בעבר או החשוד
- גידולים ממאירים הנוכחיים או החשודים באסטרוגן (למשל סרטן רירית הרחם)
- דימום באברי המין לא מאובחן
- היפרפלזיה רירית הרחם לא מטופלת
- טרומבואמבוליזם ורידי אידיופטי בעבר או עדכני (פקקת ורידים עמוקים, תסחיף ריאתי)
- רגישות יתר ידועה לחומר הפעיל או לאחד ממרכיבי התכשיר
- פורפיריה
04.4 אזהרות מיוחדות ואמצעי זהירות מתאימים לשימוש
לטיפול בסימפטומים לאחר גיל המעבר, יש להתחיל בטיפול הורמונלי חלופי (HRT) רק אם התסמינים הם כאלה שהם משפיעים לרעה על איכות החיים. בכל המקרים, יש לבצע "ניתוח תועלת וסיכון זהיר לפחות אחת לשנה, ולהמשיך ב- HRT רק אם היתרונות עולים על הסיכונים.
בדיקה / מעקב קליני
לפני תחילת או החזרת HRT, יש להעריך היסטוריה רפואית מלאה ומשפחתית מלאה. הבדיקה הכללית והגינקולוגית (כולל הבדיקה הגופנית של האגן והשדיים) חייבת להיות מונחית על פי ההיסטוריה הקלינית ועל פי התוויות ההתייחסות והאזהרות לשימוש בתרופה. במהלך הטיפול מומלץ לבצע בדיקות קליניות תקופתיות שאת תדירותן ואופיין יש להתאים לכל אישה. יש לייעץ למטופלים לדווח לרופא על כל שינוי בחזה (ראה "סרטן השד" להלן). יש לבצע בדיקות קליניות, כולל ממוגרפיה, בהתאם לפרוטוקולים הקליניים המקובלים כיום ולצרכים הקליניים של המקרה האישי.
תנאים הדורשים בקרה מיוחדת
במקרה בו יופיעו כל אחד מהמצבים הבאים, שבאו לידי ביטוי בעבר ו / או החמירו במהלך הריון או טיפול הורמונלי קודם, מומלץ להעריך היטב את האישה. יצוין כי מצבים אלה עלולים לחזור על עצמם או להחמיר במהלך הטיפול ב- Vagifem, בפרט:
- ליאומיומה (שריר הרחם) או אנדומטריוזיס
- היסטוריה או גורמי סיכון למחלות טרומבואמבוליות (ראה להלן)
- יתר לחץ דם
- hepatopathies (למשל אדנומה בכבד)
- סוכרת עם או בלי סיבוכים בכלי דם
- כולתיאטיס
- מיגרנה או כאב ראש (חמור)
- זאבת מערכתית
- היסטוריה של היפרפלזיה רירית הרחם (ראה להלן)
- אפילפסיה
- אסטמה
- אוטוסקלרוזיס
בשל הניהול המקומי של Vagifem והריכוזים הנמוכים של אסטרדיול הכלולים בו, הסיכוי להישנות או החמרה של התנאים לעיל פחות סביר ממה שנצפה בטיפול מערכתי באסטרוגן.
סיבות להפסקת הטיפול באופן מיידי
יש להפסיק את הטיפול אם יש התוויות נגד ובמצבים הבאים:
- צהבת והידרדרות בתפקודי הכבד - עלייה משמעותית בלחץ הדם
- הופעת כאב ראש דמוי מיגרנה
- הריון
היפרפלזיה רירית הרחם
נשים עם רחם שלם עם דימום לא תקין של אטיולוגיה לא בטוחה או נשים עם רחם שלם שטופלו בעבר באסטרוגנים לא מאוזנות צריכות להעריך בקפידה לגירוי יתר / ניאופלזמה ממאירה של רירית הרחם לפני תחילת הטיפול ב- Vagifem. היפרפלזיה רירית הרחם והקרצינומה מוגברת לאחר מתן אוראלי של אסטרוגן בלבד לתקופות ממושכות (ראה סעיף 4.8). תוספת של פרוגסטוגן במשך 12 ימים לפחות של המחזור בנשים שאינן כריתות רחם מפחיתה באופן משמעותי את הסיכון הזה. מינון האסטרדיול ב- Vagifem נמוך והטיפול מקומי. אצל חלק מהחולים עלולה להתרחש ספיגה מערכתית צנועה. עם זאת, טיפול ב- Vagifem אינו קשור לסיכון מוגבר להיפרפלזיה רירית הרחם או לקרצינומה של הרחם. מכיוון ש"לא נצפות השפעות מערכתיות במהלך טיפול אסטרוגני מקומי ב- Vagifem, הבחירה של "כל תוספת של הפרוגסטוגן נדחה להערכת הרופא.
באופן כללי, אין לרשום טיפול החלפת אסטרוגן למשך יותר משנה אחת מבלי לבצע הערכה קלינית נוספת כולל בדיקה גינקולוגית. אם מתרחשים דימומים ונקודות פריצה בחודשי הטיפול הראשונים או אם פרקים כאלה מופיעים לאחר זמן מה מתחילת הטיפול, או ממשיכים לאחר הפסקת הטיפול, יש לברר את הסיבה לתופעות אלה; גם באמצעות ביופסיה של " אנדומטריום שמטרתו לא לכלול ניאופלזמות ממאירות של רירית הרחם. גירוי אסטרוגן לא מאוזן עלול להוביל לשינוי מוקדם או ממאיר של מוקדי האנדומטריוזיס. הוספה של פרוגסטוגנים ל- HRT רק לאסטרוגן מומלצת אפוא בנשים שעוברות כריתת רחם לאנדומטריוזיס. במיוחד במקרה של שיורית. אנדומטריוזיס.
Vagifem הוא תכשיר מקומי במינון נמוך של אסטרדיול, ולכן הסיכוי להישנות התנאים הבאים פחות סביר מאשר בטיפול מערכתי באסטרוגנים.
סרטן השד
ניסוי קליני אקראי מבוקר פלצבו, מחקר ה- Initiative הבריאות לנשים (WHI) ומחקרים אפידמיולוגיים כולל מחקר מיליון נשים (MWS) הראו סיכון מוגבר לסרטן השד בקרב נשים שנטלו תכשירים המבוססים על סרטן השד עבור רבים שנים. אסטרוגן, או שילובי אסטרוגן-פרוגסטוגן או טיבולון ל- HRT (ראה סעיף 4.8). לכל התרופות המפורטות ב- HRT, סיכון עודף מתגלה תוך שנים אחדות של שימוש ועולה עם משך השימוש אך חוזר לתחילת המחקר תוך מספר דקות. (לכל היותר חמש) שנים לאחר הפסקת הטיפול. ב- MWS, הסיכון היחסי לסרטן השד עם אסטרוגנים סוסים מצומדים (CEE) או אסטרדיול (E2) היה גבוה יותר כאשר נוספה פרוגסטוגן הן במשטר עוקב והן במשטר מתמשך ללא קשר לסוג פרוגסטין. לא נמצאו עדויות לסיכון שונה בין דרכי הניהול השונות. במחקר WHI, מתן טיפול משולב רציף של אסטרוגן סוסים מצומדות ומדרוקסיפוגסטרון אצטט (CEE + MPA) היה קשור לסרטן שד שהיו מעט גדולים יותר, והיו להם גרורות תכופות יותר. בבלוטות לימפה מקומיות מאשר פלסבו HRT, במיוחד שילוב אסטרוגן-פרוגסטגן, מגביר את צפיפות תמונות הממוגרפיה העלולות להשפיע לרעה על הגילוי הרדיולוגי של סרטן השד.
טרומבואמבוליזם ורידי
HRT קשורה לסיכון יחסי מוגבר לפתח טרומבואמבוליזם ורידי (VTE), כלומר פקקת ורידים עמוקים או תסחיף ריאתי. ניסוי מבוקר אקראי ומחקרים אפידמיולוגיים הראו סיכון מוגבר פי 2 עד 3 בנשים הנוטלות טיפול הורמונאלי בהשוואה לנשים שאינן משתמשות ב- HRT. באחרונה, ההערכה היא שמספר המקרים של טרומבואמבוליזם ורידי שיתרחשו במשך 5 שנים הוא כ -3 מקרים ל -1000 נשים בגילאי 50 עד 59 שנים, ו -8 ל -1000 נשים בגילאי 60 עד 69 שנים. ההערכה היא כי אצל נשים בריאות שמשתמשות ב- HRT למשך 5 שנים, מספר המקרים הנוספים של טרומבואמבוליזם ורידי לאורך תקופה של 5 שנים הוא 2-6 מקרים (ההערכה הטובה ביותר = 4) לכל 1000 נשים בגילאי 50-59 שנים ו 515 מקרים (ההערכה הטובה ביותר = 9) ל -1000 נשים בגילאי 60-69. אירועים אלה נוטים יותר להתרחש בשנה הראשונה ל- HRT מאשר בשנים שלאחר מכן. גורמי סיכון מוכרים בדרך כלל לתרומבואמבוליזם ורידי הם כוללים: משפחה או היסטוריה אישית, השמנת יתר חמורה (BMI> 30 ק"ג / מ"ר), זאבת מערכתית. אין קונצנזוס לגבי התפקיד האפשרי של דליות בתרומבואמבוליזם ורידי לחולים עם היסטוריה של טרומבואמבוליזם ורידי או עם מצבים טרומבופיליים ידועים יש סיכון מוגבר לתרומבואמבוליזם ורידי. יש להעריך היטב "היסטוריה אישית או משפחתית של פרקים תרומבואמבוליים, או הפלות ספונטניות חוזרות ונשנות, על מנת לא לשלול נטייה לפקקת. עד" בוצעה הערכה מלאה של גורמים טרומבופיליים או התחלת טיפול נוגדי קרישה, יש צורך בשימוש ב- HRT בנשים כאלה. יראו אותו כמתנגד. נשים שכבר מטופלות בנוגדי קרישה דורשות הערכה מדוקדקת של יחס התועלת / סיכון של HRT.
הסיכון לתרומבואמבוליזם ורידי עשוי "להיות מוגבר באופן זמני במקרה של אי תנועה ממושכת, טראומה או ניתוח גדול. כמו בכל החולים, בתקופה שלאחר הניתוח יש לשים לב במיוחד לאמצעי מניעה שמטרתם למנוע פרקים של טרומבואמבוליזם ורידי הנובע מניתוח. כאשר צפי לאינובליציה ממושכת לאחר ניתוח אלקטיבי, במיוחד ניתוח בטן או ניתוח אורטופדי בגפיים התחתונות, יש לשקול הפסקת טיפול הורמונלי זמני במידת האפשר 4-6 שבועות לפני הניתוח.
אם מתפתחת טרומבואמבוליזם ורידי לאחר תחילת הטיפול, יש להפסיק את התרופה. יש לייעץ לנשים לפנות לרופא המטפל במידה ומתרחשים תסמינים המתייחסים לתרומבואמבוליזם ורידי (למשל גפיים תחתונות נפוחות וכואבות, כאבים פתאומיים בחזה, קוצר נשימה),
מחלת לב כלילית (CAD)
ניסויים מבוקרים אקראיים לא מראים שום תועלת קרדיווסקולרית בטיפול משולב רציף עם אסטרוגנים מצומדים ואצטט medroxyprogeserone (MPA). שני ניסויים קליניים גדולים (WHI ו- HERS או מחקר החלפת לב ואסטרוגן / פרוגסטין) מראים סיכון מוגבר לתחלואה קרדיווסקולרית בשנה הראשונה לטיפול ואין תועלת כוללת. עבור סוגים אחרים של HRT קיימים נתונים מוגבלים בלבד. מאקראי. ניסויים מבוקרים שבדקו את ההשפעות על תחלואה או תמותה קרדיווסקולארית. לפיכך, ניתן לשאול האם ניתן להרחיב מסקנות אלו גם ל- HRT עם מוצרים אחרים.
ניסוי קליני אקראי גדול (WHI-trial) הראה, כאפקט משני, סיכון מוגבר לשבץ איסכמי בקרב נשים בריאות במהלך טיפול משולב רציף עם אסטרוגנים מצומדים ו- MPA. בנשים שאינן מטופלות ב- HRT, מספר מקרי השבץ שיכולים להתרחש לאורך תקופה של 5 שנים מוערך סביב 3 לכל 1000 נשים בגילאי 50-59 ו -11 לכל 1000 נשים בגילאי 60-69. ההערכה היא כי עבור נשים המשתמשות באסטרוגן מצומד וב- MPA במשך 5 שנים, מספר המקרים הנוספים הוא בין 0 ל -3 (ההערכה הטובה ביותר = 1) לכל 1000 נשים בגילאי 50-59 ובין 1 ל -9 (ההערכה הטובה ביותר = 4) לכל 1000 נשים בגילאי 60-69. לא ידוע אם סיכון מוגבר זה מתייחס גם ל- HRT עם מוצרים אחרים.
בחלק מהמחקרים האפידמיולוגיים הוכח במחקרים אפידמיולוגיים כי טיפול ארוך טווח (לפחות 5-10 שנים) ב- HRT לאסטרוגן בלבד בנשים עם הרחם. לא בטוח אם טיפול HRT ארוך טווח עם מוצרים משולבים כרוך בתרופה אחרת. סיכון מהנוכחות עם אסטרוגן בלבד.
דמנציה
אין עדות חותכת לשיפור התפקוד הקוגניטיבי .מחקר WHI יש עדויות לעלייה בסיכון לדמנציה סבירה אצל נשים המתחילות טיפול משולב רציף באסטרוגן (CEE) + MPA לאחר גיל 65.. לא ידוע אם ממצאים אלה חלים על נשים צעירות לאחר גיל המעבר או על מוצרי HRT אחרים. מצבים אחרים אסטרוגנים עלולים לגרום לאגירת מים, ועל כן מומלץ לעקוב בקפידה אחר נשים הסובלות ממחלות לב או מחלות כליות. נשים עם אי ספיקת כליות סופנית יש להקפיד על תשומת לב מיוחדת שכן "סביר לצפות לעלייה בריכוזים במחזור הדם. של חומרים פעילים. הכלול ב- Vagifem.
תנאים אחרים
יש לעקוב מקרוב אחרי נשים הסובלות מהיפרטריגליצרידמיה לאורך כל תקופת הטיפול באסטרוגן או טיפול הורמונלי. מאז ", במצב זה, דווחו מקרים של עלייה חדה בריכוזי הפלזמה של טריגליצרידים וכתוצאה מכך דלקת הלבלב בעקבות טיפול באסטרוגן.
אסטרוגן מגביר את רמות ה- TBG, הגלובולין המחייב את בלוטת התריס, וכתוצאה מכך עלייה ברמות המחזוריות של סך הורמוני בלוטת התריס, הנמדדת כיוד קשור לחלבון, רמות T4 (על ידי כרומטוגרפיה של עמודים או בדיקת רדיואימוניות) או רמות T3 (על ידי בדיקה רדיואימונית). קליטת שרף של T3 "מופחתת: הדבר משקף את" העלייה ב- TBG. חלקים חופשיים של T4 ו- T3 נותרים ללא השפעה. חלבונים אחרים המחייבים בסרום כגון גלובולין המחייב קורטיקוסטרואידים (CBG) עשויים להיות מוגברים גם בסרום. הורבול המין מחייב גלובולין ( SHBG), מה שגורם לעלייה ברמות המחזוריות של סטרואידים והורמוני מין, בהתאמה. ריכוזי הורמונים חופשיים או פעילים ביולוגית אינם משתנים. חלבוני פלזמה אחרים עשויים להיות מוגברים (מצע אנגיוטנסינוגן / רנין, אלפא- Iantitrypsin, ceruloplasmin).
מידע על חלק ממרכיבי Vagifem
Vagifem מכיל לקטוז: חולים עם בעיות תורשתיות נדירות של אי סבילות לגלקטוז, מחסור בלקטאז או ספיגה של גלוקוז / גלקטוז לא צריכים לקחת תרופה זו.
04.5 אינטראקציות עם מוצרי תרופות אחרים וצורות אינטראקציה אחרות
מאחר "המינונים הנמוכים של אסטרדיול הכלולים ב- Vagifem ניתנים באופן מקומי, לא צפויות אינטראקציות רלוונטיות מבחינה קלינית.
04.6 הריון והנקה
הֵרָיוֹן
Vagifem אינו מסומן במהלך ההריון. אם מתרחש הריון במהלך הטיפול ב- Vagifem, יש להפסיק את הטיפול באופן מיידי. התוצאות של רוב המחקרים האפידמיולוגיים על חשיפה עוברית לא רצונית לאסטרוגן מעידות כי אין השפעה טרטוגנית או foetotoxic.
זמן האכלה
Vagifem אינו מסומן במהלך הנקה.
04.7 השפעות על יכולת הנהיגה וההתנהלות במכונות
אין השפעות ידועות.
04.8 תופעות לא רצויות
יותר מ -640 מטופלים טופלו ב- Vagifem בניסויים קליניים שונים, כולל מעל 200 חולים שטופלו במשך 28-64 שבועות.אירועי לוואי הקשורים בהחלט למתן אסטרוגנים שהתרחשו בשכיחות גבוהה בקבוצת הטיפול בהשוואה לחולים שאינם מטופלים (פלסבו), מסווגים כ"נפוצים (> 1/100;
שיעור הגילוי הספונטני של תופעות לוואי הקשורות ל- Vagifem הוא כ -1 מקרה לכל 10,000 מטופלים / שנה. אירועים שליליים שלא נמצאה להם תדירות מוגברת בניסויים קליניים, אך אשר דווחו באופן ספונטני ואשר על דעתם פה אחד יש לקחת בחשבון שהם קשורים אולי לכן הטיפול ב- Vagifem מסווג כ"נדיר מאוד (
הניסיון שלאחר השיווק אינו "כפוף לדיווח, במיוחד לתגובות שליליות קלות וכבר מוכרות. לכן יש לפרש את התדרים המוצגים לאור האמור לעיל.
תופעות הלוואי השליליות המדווחות ביותר הן: דימום והפרעות בנרתיק. תופעות לוואי הקשורות לטיפול באסטרוגן כגון כאבי שד, בצקת היקפית ודימום לאחר גיל המעבר מופיעים ככל הנראה רק בתחילת הטיפול ב- Vagifem.
תגובות הלוואי הבאות דווחו בשיתוף עם טיפול באסטרוגן:
- אוטם בשריר הלב ומחלות לב
- כולתיאטיס
- הפרעות עור ורקמות תת עוריות: קלואזמה, אריתמה רב -צורנית, אריתמה נודוסום, פורפורת כלי הדם, גירוד
- קנדידה נרתיקית
- סיכון לפתח סרטן רירית הרחם (ראה סעיף 4.4),
- היפרפלזיה רירית הרחם או הגדלת שרירנים ברחם *
- טרומבואמבוליזם ורידי
- נדודי שינה
- אפילפסיה
- הפרעות בחשק המיני
- החמרה באסתמה
- דמנציה אפשרית (ראה סעיף 4.4)
* בנשים שאינן כירורגיות בהיסטריה התגובות השליליות הבאות דווחו עם HRT מערכתית של אסטרוגן או אסטרוגן פרוגסטגן:
* סרטן השד
על פי עדויות ממספר רב של מחקרים אפידמיולוגיים וממחקר אקראי מבוקר פלסבו, יוזמת בריאות האישה (WHI), הסיכון הכולל לסרטן השד עולה עם הגדלת משך השימוש ב- HRT בחולים המטופלים ובאלו שעברו לאחרונה השתמשתי בזה.
לגבי HRT לאסטרוגן בלבד, ההערכה היא כי הסיכון היחסי (RR) מוכיח ניתוח חוזר של הנתונים המקוריים מ -51 מחקרים אפידמיולוגיים (בהם יותר מ -80% מהטיפולים להחלפת הורמונים היו באסטרוגן בלבד) וממקור מחקר אפידמיולוגי של מיליון נשים (MWS), הוא דומה ל -1.35 (95% CI 1.21-1.49) ול -1.30 (95% CI 1.21-1.40) בהתאמה.
עבור HRT משולב עם אסטרוגן פלוס פרוגסטוגנים, מספר מחקרים אפידמיולוגיים דיווחו על סיכון גבוה יותר לסרטן השד בהשוואה לאסטרוגן בלבד.
מחקר ה- MWS דיווח כי השימוש בסוגים שונים של HRT אסטרוגן -פרוגסטגן משולב היה קשור לסיכון גבוה יותר לסרטן השד בהשוואה לנשים שמעולם לא קיבלו טיפול (RR = 2.00, 95% CI: 1.88 - 2.12) בהשוואה לשימוש ב- אסטרוגן בלבד (RR = 1.30, 95% CI: 1.21 - 1.40) או שימוש בטיבולון (RR = 1.45; 95% CI 1.25 - 1.68).
מחקר WHI דיווח על סיכון מוערך של 1.24 (95% CI 1.01 - 1.54) לאחר 5.6 שנים של טיפול משולב באסטרוגן -פרוגסטוגן HRT (EEC + MPA) בכל המשתמשים בהשוואה לפלסבו.
הסיכונים המוחלטים המחושבים על ידי מחקרי MWS ו- WHI מוצגים להלן:
ה- MWS העריך, בהתבסס על השכיחות הממוצעת הידועה של סרטן השד במדינות מפותחות, כי:
• עבור נשים שאינן משתמשות ב- HRT, כ -32 מתוך 1000 נשים צפויות להיות מאובחנות כחולות סרטן השד בגילאי 50 עד 64. עבור 1000 נשים שמשתמשות או השתמשו לאחרונה ב- HRT, מספר המקרים הנוספים בתקופה המקבילה יהיה:
למשתמשי טיפול תחליפי אסטרוגן בלבד
בין 0 ל -3 (ההערכה הטובה ביותר = 1.5) לשימוש 5 שנים
בין 3 ל -7 (ההערכה הטובה ביותר = 5) לשימוש של 10 שנים.
עבור משתמשים בשילוב של אסטרוגן בתוספת HRT של פרוגסטוגן
בין 5 ל -7 (ההערכה הטובה ביותר = 6) לשימוש של 5 שנים
בין 18 ל -20 (ההערכה הטובה ביותר = 19) לשימוש של 10 שנים
מחקר ה- WHI העריך כי לאחר 5.6 שנים של מעקב אחר נשים בגילאי 50 עד 79 שנים, 8 מקרים נוספים פולשניים של סרטן שד לכל 10,000 נשים בשנה יובאו משילוב משולב של אסטרוגן-פרוגסטוגן (CEE + MPA). על פי החישובים המוחזרים מנתוני המחקר הקליני, ההערכה היא כי:
* עבור 1000 נשים בקבוצת הפלסבו,
או כ -16 מקרים של סרטן שד פולשני יאובחנו תוך 5 שנים
* עבור 1000 נשים שהשתמשו באסטרוגן משולב + פרוגסטוגן HRT (CEE + MPA), מספר המקרים הנוספים יהיה
בין 0 ל -9 (ההערכה הטובה ביותר = 4) לשימוש במשך 5 שנים
מספר המקרים הנוספים של סרטן השד בקרב נשים המשתמשות ב- HRT דומה באופן כללי לכל הנשים המתחילות ב- HRT ללא קשר לגיל תחילת הטיפול (בין 45 ל -65) (ראה סעיף 4.4).
סרטן רירית הרחם
בנשים עם רחם שלם, הסיכון להיפרפלזיה רירית הרחם ולסרטן רירית הרחם עולה עם הגדלת משך השימוש באסטרוגן לא מאוזן. על פי נתוני מחקרים אפידמיולוגיים, האומדן הטוב ביותר של הסיכון הוא שאצל נשים שאינן משתמשות ב- HRT, כ -5 מקרים של סרטן רירית הרחם צפויים להיות מאובחנים בכל 1,000 נשים בגילאי 50 עד 65. בהתאם למשך הטיפול ומינון האסטרוגן, הסיכון המוגבר לחלות בסרטן רירית הרחם בקרב נשים המשתמשות באסטרוגן לא מאוזן גדול פי 2 עד 12 מאשר באלו שלא.
הוספת פרוגסטוגן לטיפול באסטרוגן בלבד מפחיתה משמעותית את הסיכון הגבוה הזה.
** טרומבואמבוליזם ורידי כגון פקקת ורידים עמוקים ברגליים או תסחיף אגן וריאתי, שכיח הרבה יותר בקרב משתמשי HRT מאשר לא משתמשים. למידע נוסף ראו סעיף 4.3 התוויות נגד ו 4.4 אזהרות ואמצעי זהירות מיוחדים לשימוש.
04.9 מנת יתר
לא דווח על מקרים של מנת יתר.
Vagifem מיועדת לטיפול תוך -וגינאלי מקומי. המינון של אסטרדיול הוא כל כך נמוך עד שיהיה צורך לתת מספר לא מבוטל של טבליות כדי לגשת למינון המשמש בדרך כלל לשימוש מערכתי. הטיפול חייב להיות סימפטומטי.
05.0 נכסים פרמקולוגיים
05.1 תכונות פרמקודינמיות
קבוצה פרמקותרפית: אסטרוגנים טבעיים וחצי סינתטיים שאינם קשורים ATC G03CA03
אסטרוגנים טבעיים וחצי סינתטיים, פשוטים (לשימוש בנרתיק). הניסוח הפעיל, ה- 17β-אסטרדיול הסינתטי, זהה מבחינה כימית וביולוגית לאסטרדיול האנושי האנדוגני. 17β-אסטרדיול אנדוגני מעורר ושומר על מאפיינים מיניים נקביים משניים ועיקריים. ההשפעה הביולוגית של 17β-אסטרדיול מתבצעת באמצעות סדרה של קולטנים ספציפיים.קומפלקס קולטן הסטרואידים נקשר לדנ"א התאי ומעורר סינתזה של חלבונים ספציפיים. התבגרות האפיתל בנרתיק תלויה באסטרוגנים. אלה מגדילים את מספר התאים השטחיים והביניים ביחס לתאים הבסיסיים. האסטרוגנים שומרים על ה- pH הנרתיק מתחת ל -4.5, מה שמעודד צמיחה של צמחיית חיידקים תקינה, כאשר Lactobacillus Döderlein דומיננטי.
05.2 "תכונות פרמקוקינטיות
תרופה אסטרוגנית נספגת היטב דרך העור, הריריות ודרכי העיכול. מתן הנרתיק של אסטרוגן עוקף את השלב המטבולי הראשון. מחקר אקראי, כפול סמיות, כפול-תקופתי, בן שני מרכזים, נערך על מנת להעריך את הפרמקוקינטיקה של Vagifem. של הטיפול, ניתן למצוא רק ספיגה שולית של 17β-אסטרדיול, עם רמות ממוצעות בטווח גיל המעבר. מחקר אחר בחולים צעירים, בגיל ממוצע 52 שנים, הראה כי יישום Vagifem בנרתיק במשך 12 שבועות גרם לממוצע אסטרדיול C של 50 pg / ml ולא נצפתה הצטברות משמעותית של אסטרדיול במונחים של AUC0. -24 (ראה טבלה 1) הריכוזים הממוצעים של 17β-אסטרדיול בכל נקודה בעקומה היו בטווח הנורמלי לאחר גיל המעבר.
פרמטרים פרמקוקינטיים ממוצעים (סטיית תקן β) לאסטרדיול
רמות האסטרון שנצפו במהלך 12 שבועות הטיפול ב- Vagifem לא הראו הצטברות והערכים שנמצאו היו בטווח הנורמלי לאחר גיל המעבר. מטבוליטים של אסטרוגנים מופרשים בעיקר בשתן כגלוקורונידים וסולפטים.
05.3 נתוני בטיחות פרה -קליניים
מכיוון ש- "17β-אסטרדיול הוא" חומר ידוע, המתואר בספרות הפרמקוטוקסיקולוגית, לא בוצעו מחקרים נוספים.
06.0 מידע פרמצבטי
06.1 מרכיבים
לוח: היפרומלוז לקטוז מונוהידראט עמילן תירס מגנזיום סטרט
ציפוי סרט: היפרומלוז מקרוגול 6000
06.2 חוסר התאמה
לא רלוונטי
06.3 תקופת תוקף
3 שנים.
06.4 אמצעי זהירות מיוחדים לאחסון
אין לאחסן מעל 25 ° C. אין לאחסן במקרר. שמור את המיכל בקרטון החיצוני.
06.5 אופי האריזה המיידית ותכולת האריזה
כל טבליה מונחת במוליך חד פעמי מפוליאתילן / פוליפרופילן חד פעמי. המריחים ארוזים בשלפוחיות PVC / אלומיניום. כל אריזה מכילה 3 שלפוחיות המורכבות כל אחת מ -5 מוליכים המכילים את הטבליות.
06.6 הוראות שימוש וטיפול
אין הוראות מיוחדות
מחזיק רשות השיווק 07.0
Novo Nordisk A / S, 2880 Bagsvaerd, דנמרק
08.0 מספר אישור השיווק
AIC n.028894018
09.0 תאריך האישור הראשון או חידוש האישור
22 באפריל 1995