רכיבים פעילים: Denosumab
פתרון Prolia 60 מ"ג להזרקה במזרק מלא
תוספות אריזה של Prolia זמינות למידות האריזה:- פתרון פרוליה 60 מ"ג להזרקה במזרק מלא
- פתרון פרוליה 60 מ"ג להזרקה
מדוע משתמשים בפרוליה? לשם מה זה?
מהי פרוליה וכיצד היא פועלת
פרוליה מכילה denosumab, חלבון (נוגדן חד שבטי) המפריע לפעולה של חלבון אחר, לטיפול באובדן עצמות ואוסטיאופורוזיס. טיפול בפרוליה הופך את העצמות לחזקות יותר ופחות מועדות לשברים.
עצם היא רקמה חיה המתחדשת ללא הרף. אסטרוגן עוזר לשמור על בריאות העצמות. לאחר גיל המעבר הפחתה ברמות האסטרוגן עלולה לגרום לעצמות דקיקות ושבירות, מה שעלול להוביל להתפתחות של מצב הנקרא אוסטאופורוזיס. אוסטאופורוזיס יכול להתרחש גם אצל גברים מסיבות שונות כולל הזדקנות ו / או רמה נמוכה של ההורמון הגברי, טסטוסטרון. לחולים רבים עם אוסטאופורוזיס אין תסמינים, אך הם עדיין נמצאים בסיכון לשברים בעצמות, במיוחד בעמוד השדרה, עצם הירך ופרקי כף היד.
ניתוחים או תרופות המפסיקות את ייצור האסטרוגן או הטסטוסטרון המשמשים לטיפול בחולים עם סרטן השד או הערמונית יכולים גם לגרום לאובדן עצם. העצמות הופכות שבירות יותר ושברות בקלות רבה יותר.
לאיזה סוג טיפול משמש פרוליה
פרוליה משמש לטיפול:
- אוסטאופורוזיס אצל נשים לאחר גיל המעבר (אוסטאופורוזיס לאחר גיל המעבר) ובגברים שיש להם סיכון מוגבר לשברים (עצמות שבורות), כדי להפחית את הסיכון לשברים בחוליות, חוליות וירכיים.
- אובדן עצם בגברים כתוצאה מירידה ברמות ההורמון (טסטוסטרון) עקב ניתוח או טיפול תרופתי בחולים עם סרטן הערמונית.
התוויות נגד כאשר אין להשתמש בפרוליה
אין להשתמש בפרוליה
- אם יש לך רמות סידן נמוכות בדם (היפוקלצמיה).
- אם אתה אלרגי ל- denosumab או לכל אחד ממרכיבי התרופה האחרים
אמצעי זהירות לשימוש מה שאתה צריך לדעת לפני נטילת Prolia
שוחח עם הרופא או הרוקח לפני השימוש בפרוליה.
במהלך הטיפול בפרוליה אתה עשוי להבחין באדמומיות ונפיחות של העור, לרוב ברגל התחתונה, עם תחושת חום וכאב (צלוליטיס) ואולי עם תסמינים של חום. דווח לרופא מיד אם אתה נתקל באחד מהתסמינים הללו.
ספר לרופא אם יש לך אלרגיה לטקס (מכסה המחט של המזרק הממולא מכיל נגזרת של לטקס).
כמו כן, עליך ליטול תוספי סידן וויטמין D בזמן הטיפול בפרוליה. הרופא שלך ידון איתך בנושא זה.
ייתכן שיש לך רמות סידן נמוכות בדם בזמן הטיפול ב- Prolia. ספר לרופא מיד אם אתה מבחין באחד מהתסמינים הבאים: עוויתות, עוויתות או התכווצויות בשרירים ו / או קהות או עקצוצים באצבעות, בהונות או סביב הפה ו / או התקפים, בלבול או אובדן הכרה.
ספר לרופא אם יש לך או סבל מבעיות כליות חמורות, פגיעה בכליות או אם עברת דיאליזה, מה שעלול להגביר את הסיכון לרמות סידן נמוכות בדם אם אינך לוקח תוספי סידן.
השפעה לא רצויה הנקראת אוסטאונקרוזיס של הלסת (ניוון עצם חמור של הלסת) דווחה לעיתים רחוקות (עשויה להשפיע על עד 1 מתוך 1,000 אנשים) בחולים המקבלים פרוליה לאוסטיאופורוזיס. אוסטאונקרוזיס של הלסת. היא יכולה להתרחש גם לאחר הפסקת הטיפול.
חשוב לנסות למנוע התפתחות אוסטאונקרוזיס של הלסת מכיוון שמדובר במצב כואב אשר יכול להיות קשה לטיפול.כדי להפחית את הסיכון להתפתחות אוסטאונקרוזיס של הלסת, עליך לנקוט באמצעי זהירות מסוימים.
לפני קבלת הטיפול, דווח לרופא או לאחותך (רופא) אם אתה:
- סובלים מבעיות בפה או בשיניים, כגון היגיינת שיניים לקויה, מחלות חניכיים או מתכננים לבצע עקירת שיניים;
- אין לך טיפול שיניים קבוע או שלא עברת בדיקת שיניים במשך זמן רב;
- אתה מעשן (מכיוון שזה עלול להגביר את הסיכון לבעיות שיניים);
- טופלו בעבר בביספוספונט (משמש לטיפול או מניעה של הפרעות בעצמות);
- אתה נוטל תרופות הנקראות קורטיקוסטרואידים (כגון פרדניזולון או דקסמתזון);
- יש סרטן.
הרופא שלך עשוי לבקש ממך לבצע בדיקת שיניים (אצל רופא השיניים) לפני תחילת הטיפול בפרוליה.
במהלך הטיפול יש צורך לשמור על היגיינת הפה ולבצע בדיקות שיניים תקופתיות. אם אתה לובש תותבות עליך לוודא שהן מוכנסות כהלכה. אם אתה עובר טיפול שיניים או מתכנן לעבור ניתוח שיניים (למשל עקירות שיניים), אנא הודע לרופא טיפולי השיניים והודיע לרופא השיניים שאתה מטופל בפרוליה.
פנה לרופא ולרופא השיניים שלך מיד אם אתה מבחין בבעיות בפה או בשיניים כגון נפילת שיניים, כאבים או נפיחות או אי ריפוי של פצעים בפה או הפרשות, מכיוון שאלו יכולים להיות סימנים לתופעת לוואי הנקראת אוסטאונקרוזיס של הלסת תחתונה / מקסימה. (ONJ).
ילדים ומתבגרים
Prolia לא מומלץ לילדים ומתבגרים מתחת לגיל 18. השימוש בפרוליה בקרב ילדים ומתבגרים לא נחקר.
אינטראקציות אילו תרופות או מזונות יכולים לשנות את ההשפעה של פרוליה
ספר לרופא או לרוקח אם אתה נוטל, נטלת לאחרונה או עשוי לקחת תרופות אחרות. חשוב במיוחד שתודיע לרופא אם אתה נוטל תרופות אחרות המכילות denosumab.
אסור ליטול את Prolia יחד עם תרופות אחרות המכילות denosumab
אזהרות חשוב לדעת כי:
פרוליה לא נחקרה בנשים בהריון. חשוב שתספר לרופא אם הינך בהריון; אם אתה חושב שאתה עלול להיות בהריון; או אם אתה מתכנן הריון.
השימוש בפרוליה אינו מומלץ אם הינך בהריון. אם הינך בהריון בעת נטילת פרוליה, אנא הודע / י לרופא / ית. יתכן ותעודד / י להשתתף בתכנית מעקב ההריון של אמגן. ניתן למצוא פרטי התקשרות מקומיים. בפסקה 6 בעלון זה.
לא ידוע אם פרוליה עוברת לחלב אם. חשוב שתודיע לרופא אם את מניקה או מתכננת להניק. לאחר מכן הרופא שלך יעזור לך להחליט אם להפסיק את ההנקה או להפסיק את נטילת פרוליה, בהתחשב ביתרון ההנקה לתינוק ובתועלת בלקיחת פרוליה לאם.
אם הינך בזמן נטילת פרוליה, אנא הודע זאת לרופא. ייתכן שתעודד אותך להשתתף בתכנית מעקב ההנקה של אמגן. פרטי התקשרות מקומיים מסופקים בסעיף 6 בעלון זה. שאל את הרופא או הרוקח שלך לייעוץ לפני השימוש בתרופה זו.
נהיגה ושימוש במכונות
לפרוליה אין השפעה או זניחה על יכולת הנהיגה או השימוש במכונות.
פרוליה מכיל סורביטול (E420)
אם אמרו לך הרופא כי יש לך "אי סבילות לסוכרים מסוימים (סורביטול E420), פנה לרופא לפני נטילת התרופה.
אם אתה על דיאטה דלת נתרן
תרופה זו מכילה פחות מ- 1 mmol נתרן (23 מ"ג) ל -60 מ"ג, כלומר "ללא נתרן".
מינון, שיטת וזמן הניהול אופן השימוש בפרוליה: מינון
המינון המומלץ הוא מזרק מלא של 60 מ"ג המנוהל אחת לשישה חודשים כזריקה אחת מתחת לעור (תת עורית). המקומות המתאימים ביותר להזרקה הם הירכיים העליונות והבטן. אם מישהו עוזר לך לתת לך את הזריקה, הוא יכול להשתמש גם בזרוע העליונה החיצונית. כל חבילת Prolia מכילה כרטיס תזכורת עם מדבקות נשלפות, שניתן להסיר מהקופסה. השתמש במדבקות הנשלפות כדי לסמן בלוח השנה שלך את התאריך של הזריקה הבאה ו / או השתמש בכרטיס התזכורת כדי לעקוב אחר תאריך ההזרקה הבאה.
כמו כן, עליך ליטול תוספי סידן וויטמין D בזמן הטיפול בפרוליה. הרופא שלך ידון איתך בנושא זה.
הרופא שלך יכול להחליט אם הכי טוב לך או למטפל להזריק פרוליה.הרופא או האחות שלך יראו לך או למטפלת כיצד לקחת פרוליה.
לפני השימוש במזרק ממולא Prolia עם מגן מחט אוטומטי, אנא קרא מידע חשוב זה:
- חשוב שלא תנסה לתת את הזריקה אלא אם קיבלת הוראות מתאימות מהרופא או מאנשי בריאות.
- פרוליה ניתנת כזריקה לרקמה ממש מתחת לעור (זריקה תת עורית).
- דווח לרופא אם אתה אלרגי לטקס (מכסה המחט במזרק הממולא מכיל נגזרת לטקס) אין להסיר את מכסה המחט האפור מהמזרק הממולא עד שמוכנים להזריק.
- אין להשתמש במזרק הממולא מראש אם הוא נפל על משטח קשיח. השתמש במזרק חדש מלא ופנה לרופא או לרופא המטפל.
- אל תנסה להפעיל את המזרק הממולא לפני ההזרקה.
- אל תנסה להסיר את מגן הבטיחות השקוף מהמזרק הממולא.
פנה לרופא או לרופא המטפל בכל שאלה.
שלב 1: הכנה
א) הסר את עטיפת המזרק הממולא מהאריזה והכן את החומרים הדרושים להזרקה: מגבוני אלכוהול, צמר גפן או כרית גזה, טלאי ומיכל סילוק חד (לא כלול).
להזרקה נוחה יותר, השאירו את המזרק הממולא בטמפרטורת החדר כ -30 דקות לפני ההזרקה. שטפו את הידיים היטב במים וסבון.
הניחו את המזרק החדש וחומרים נחוצים אחרים על משטח עבודה נקי ומואר היטב.
- אל תנסה לחמם את המזרק באמצעות מקור חום כגון מים חמים או מיקרוגל.
- אין להשאיר את המזרק הממולא חשוף לאור שמש ישיר. לא.
- אין לנער את המזרק הממולא יתר על המידה.
- שמור את המזרק הממולא הרחק מעיני ילדים.
ב) פתח את השקיק, קרע את המכסה. אחז במגן הבטיחות של המזרק הממולא כדי להסיר את המזרק הממולא מהתיק.
מטעמי אבטחה:
- אל תפוס את הבוכנה.
- אל תפוס את מכסה המחט האפור.
ג) בדוק את התרופה ואת המזרק הממולא.
- אין להשתמש במזרק הממולא אם:
- התרופה עכורה או שיש בה חלקיקים. היא צריכה להיות תמיסה בהירה, חסרת צבע עד צהוב מעט.
- חלקים מסוימים נראים סדוקים או שבורים.
- מכסה המחט האפור חסר או אינו מחובר היטב.
- תאריך התפוגה המודפס על התווית עבר את היום האחרון בחודש המצוין.
בכל המקרים יש לפנות לרופא או לרופא המטפל.
שלב 2: הכנה
א) לשטוף את הידיים ביסודיות. הכינו ונקו את אתר ההזרקה.
יכול להשתמש:
- החלק העליון של הירך.
- הבטן, למעט שטח של 5 סנטימטרים ממש סביב הטבור.
- הזרוע העליונה החיצונית (רק אם מישהו אחר נותן לך את הזריקה).
- נקה את מקום ההזרקה בעזרת מגבון אלכוהול. השאר את העור יבש.
- אין לגעת באתר ההזרקה לפני ההזרקה.
- אין להזריק לאזורים בהם העור רגיש, פצוע, אדום או קשה. הימנע מהזרקה לאזורים עם צלקות או סימני מתיחה.
ב) משוך בזהירות את מכסה המחט האפור החוצה והתרחק מגופך
ג) הרם את אתר ההזרקה ליצירת משטח יציב.
- חשוב לשמור על צביעת העור במהלך ההזרקה
שלב 3: הזרקה
א) שמור את העור צובט. הכנס את המחט לעור
- אין לגעת באזור הנקי של העור
ב) דחוף את הבוכנה בלחץ איטי ויציב עד שאתה מרגיש או שומע "קליק". דחוף את כל הדרך פנימה עד שהוא ילחץ
- חשוב לדחוף כל הדרך עד ה"טאק "כדי להזריק את המינון המלא.
ג) שחרר את האגודל. לאחר מכן הרחיק את המזרק מהעור שלך
לאחר שחרור הבוכנה, מגן הבטיחות של המזרק הממולא יכסה את מחט ההזרקה בצורה מאובטחת.
- אין להחזיר את מכסה המחט האפור על מזרקים משומשים שטופלו.
שלב 4: סיים
A זרוק את המזרק הממולא המשומש וחומרים אחרים בכלי לסילוק חד.
יש להיפטר מתרופות בהתאם לתקנות המקומיות. שאל את הרוקח כיצד לזרוק תרופות שאינך משתמש בהן יותר. אמצעים אלה יסייעו בהגנה על הסביבה.
שמור את המזרק ומיכל סילוק החדים הרחק מעיני ילדים.
- אין לעשות שימוש חוזר במזרק הממולא.
- אין למחזר מזרקים מלאים או להשליך אותם לפסולת ביתית.
ב) בדוק את אתר ההזרקה.
אם אתה מבחין בדם, לחץ על צמר גפן או גזה מעל אתר ההזרקה. אין לשפשף את אתר ההזרקה. במידת הצורך, מרחי תיקון.
מנת יתר מה לעשות אם נטלת יותר מדי פרוליה
אם שכחת לקחת פרוליה
אם החמצת מנה של פרוליה, יש לתת את ההזרקה בהקדם האפשרי.לאחר מכן יש לתת את הזריקות כל 6 חודשים מיום הזריקה האחרונה.
אם תפסיק לקחת פרוליה
כדי להפיק את המרב מהטיפול שלך, חשוב שתיקח את Prolia כל עוד הרופא שלך קובע זאת. התייעץ עם הרופא שלך לפני שאתה שוקל להפסיק את הטיפול.
תופעות לוואי מהן תופעות הלוואי של פרוליה
כמו כל התרופות, תרופה זו עלולה לגרום לתופעות לוואי, אם כי לא כולם מקבלים אותן.
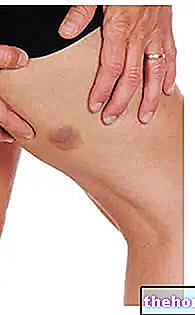
באופן לא נדיר, חולים המטופלים בפרוליה עלולים לפתח זיהומים בעור (בעיקר צלוליטיס). דווח לרופא מיד אם אתה נתקל באחד מהתסמינים הללו בעת נטילת פרוליה: אדמומיות ונפיחות בעור, לרוב ברגל התחתונה, עם תחושת חום וכאבים ואולי סימפטומים של חום.
לעיתים נדירות, מטופלים המטופלים בפרוליה עלולים לפתח כאבים בפה ו / או בלסת, נפיחות או נגעים שאינם מרפאים בפה או בלסת, הפרשות, קהות או תחושת כבדות בלסת / לסת או התנודדות של שן. אלה יכולים להיות סימנים לניוון עצמות חמור של הלסת (אוסטאונקרוזיס). ספר לרופא ולרופא השיניים שלך מיד אם אתה נתקל בסימפטומים כאלה במהלך הטיפול בפרוליה או לאחר הפסקת הטיפול.
לעיתים נדירות, לחולים המטופלים בפרוליה עלולות להיות רמות סידן נמוכות בדם (היפוקלצמיה). התסמינים כוללים התכווצויות שרירים, עוויתות או התכווצויות ו / או קהות או עקצוצים באצבעות, בהונות או סביב הפה ו / או התקפים, בלבול או אובדן הכרה. צור קשר עם הרופא שלך מיד אם אחד מהתסמינים הללו מופיע. רמות נמוכות של סידן בדם יכולות גם להוביל לשינוי בקצב הלב הנקרא הארכת מרווח QT, הנראה באלקטרוקרדיוגרפיה (א.ק.ג.).
תופעות לוואי שכיחות מאוד (עשויות להשפיע על יותר מ -1 מתוך 10 אנשים):
- כאבים בעצמות, במפרקים ו / או בשרירים לפעמים קשים,
- כאבים בידיים או ברגליים (כאבים בגפיים).
תופעות לוואי שכיחות (עשויות להשפיע על עד 1 מתוך 10 אנשים):
- צורך תכוף וכואב להעביר שתן, דם בשתן, בריחת שתן,
- דלקות בדרכי הנשימה העליונות,
- כאב, עקצוץ או קהות המקרינים לגפיים התחתונות (סיאטיקה),
- עכירות בעדשה (קטרקט),
- עצירות,
- אי נוחות בבטן,
- פריחה,
- גירוד, אדמומיות ו / או יובש בעור (אקזמה).
תופעות לוואי לא שכיחות (עשויות לפגוע בעד אחד מכל 100 אנשים):
- חום, הקאות וכאבי בטן או אי נוחות בבטן (דיברטיקוליטיס),
- דלקות אוזניים.
תופעות לוואי נדירות (עשויות להופיע בקרב עד 1 מתוך 1,000 אנשים):
- תגובות אלרגיות (למשל נפיחות בפנים, בשפתיים, בלשון, בגרון או בחלקים אחרים של הגוף; פריחה, גירוד, כוורות, צפצופים או קשיי נשימה).
שברים נדירים של עצם הירך עלולים להתרחש לעתים רחוקות.
צור קשר עם הרופא שלך אם אתה חווה כאב חדש או יוצא דופן בירך, במפשעה או בירך במהלך הטיפול בפרוליה, מכיוון שזה יכול להיות סימן מוקדם לשבר אפשרי של עצם הירך.
אם אתה נתקל בתופעות לוואי כלשהן, שוחח עם הרופא או הרוקח. זה כולל כל תופעות לוואי אפשריות שאינן מופיעות בעלון זה.
דיווח על תופעות לוואי
אם אתה נתקל בתופעות לוואי כלשהן, שוחח עם הרופא או הרוקח. זה כולל כל תופעות לוואי אפשריות שאינן מופיעות בעלון זה. תוכל גם לדווח על תופעות לוואי ישירות באמצעות מערכת הדיווח הלאומית הרשומה בנספח V. על ידי דיווח על תופעות לוואי תוכל לסייע לספק מידע נוסף אודות בטיחותה של תרופה זו.
תפוגה ושמירה
שמור את התרופה הרחק מעיני ילדים.
אין להשתמש בתרופה זו לאחר תאריך התפוגה המופיע על התווית והקרטון לאחר תאריך התפוגה. תאריך התפוגה מתייחס ליום האחרון של אותו חודש.
שומרים במקרר (2 ° C - 8 ° C).
אל תקפא.
יש לאחסן באריזה המקורית כדי להגן על התרופה מפני אור.
אין לנער יתר על המידה.
ניתן להשאיר את המזרק הממולא מחוץ למקרר כדי להגיע לטמפרטורת החדר (עד 25 מעלות צלזיוס) לפני ההזרקה. הדבר יהפוך את הזריקה לנוחה יותר.לאחר שהמזרק הגיע לטמפרטורת החדר (עד 25 מעלות צלזיוס), יש להשתמש בו תוך 30 יום.
אין לזרוק תרופות דרך שפכים או פסולת ביתית. שאל את הרוקח כיצד עליך לזרוק תרופות שאינך משתמש בהן יותר. הדבר יעזור להגן על הסביבה.
6. תכולת החבילה ומידע נוסף
מה פרוליה מכיל
- המרכיב הפעיל הוא denosumab. כל מזרק מלא של 1 מ"ל מכיל 60 מ"ג של denosumab (60 מ"ג / מ"ל).
- המרכיבים הנוספים הם חומצה אצטית קרחונית, נתרן הידרוקסיד, סורביטול (E420), פוליסורבט 20 ומים להזרקות.
איך נראית פרוליה ותכולת האריזה
פרוליה היא פתרון בהיר, חסר צבע עד צהוב מעט להזרקה במזרק מלא המיועד לשימוש.
כל אריזה מכילה מזרק ממולא אחד עם מגן מחט. כל אריזה מכילה מזרק מלא אחד.
חָשׁוּב
לפני השימוש במזרק ממולא Prolia עם מגן מחט אוטומטי, אנא קרא מידע חשוב זה:
- חשוב שלא תנסה לתת את הזריקה אלא אם קיבלת הוראות מתאימות מהרופא או מאנשי בריאות.
- פרוליה ניתנת כזריקה לרקמה ממש מתחת לעור (זריקה תת עורית).
- ספר לרופא אם אתה אלרגי לטקס (מכסה המחט במזרק הממולא מכיל נגזרת של לטקס).
- אין להסיר את מכסה המחט האפור מהמזרק הממולא עד שמוכנים להזריק.
- אין להשתמש במזרק הממולא מראש אם הוא נפל על משטח קשיח. השתמש במזרק חדש מלא ופנה לרופא או לרופא המטפל.
- אל תנסה להפעיל את המזרק הממולא לפני ההזרקה.
- אל תנסה להסיר את מגן הבטיחות השקוף מהמזרק הממולא.
פנה לרופא או לרופא המטפל בכל שאלה.
שלב 1: הכנה
א הוציאו את עטיפת המזרק הממולא מהאריזה והכינו את החומרים הדרושים להזרקה: מגבוני אלכוהול, משטח צמר גפן או כרית גזה, טלאי ומיכל סילוק חד (לא כלול).
להזרקה נוחה יותר, השאירו את המזרק הממולא בטמפרטורת החדר כ -30 דקות לפני ההזרקה. שטפו את הידיים היטב במים וסבון.
הניחו את המזרק החדש וחומרים נחוצים אחרים על משטח עבודה נקי ומואר היטב.
- אל תנסה לחמם את המזרק באמצעות מקור חום כגון מים חמים או מיקרוגל.
- אין להשאיר את המזרק הממולא חשוף לאור שמש ישיר.
- אין לנער את המזרק הממולא יתר על המידה.
- שמור את המזרק הממולא הרחק מעיני ילדים.
B פתח את העטיפה, קרע את המכסה. אחז במגן הבטיחות של המזרק הממולא כדי להסיר את המזרק הממולא מהאריזה.
מטעמי אבטחה:
- אל תפוס את הבוכנה.
- אל תפוס את מכסה המחט האפור.
ב בדוק את התרופה ואת המזרק הממולא.
אין להשתמש במזרק הממולא אם:
- התרופה עכורה או שיש בה חלקיקים. היא צריכה להיות תמיסה בהירה, חסרת צבע עד צהוב מעט.
- חלקים מסוימים נראים סדוקים או שבורים.
- מכסה המחט האפור חסר או אינו מחובר היטב.
- תאריך התפוגה המודפס על התווית עבר את היום האחרון בחודש המצוין.
בכל המקרים יש לפנות לרופא או לרופא המטפל.
שלב 2: הכנה
א לשטוף את הידיים ביסודיות. הכינו ונקו את אתר ההזרקה. יכול להשתמש:
- החלק העליון של הירך. זרוע עליונה בטן ירך עליונה
- הבטן, למעט שטח של 5 סנטימטרים ממש סביב הטבור.
- הזרוע העליונה החיצונית (רק אם מישהו אחר נותן לך את הזריקה).
נקה את מקום ההזרקה בעזרת מגבון אלכוהול. השאר את העור יבש.
- אין לגעת באתר ההזרקה לפני ההזרקה.
- אין להזריק לאזורים בהם העור רגיש, פצוע, אדום או קשה. הימנע מהזרקה לאזורים עם צלקות או סימני מתיחה.
B הסר בזהירות את מכסה המחט האפור כלפי חוץ והתרחק מגופך.
ג הרם את אתר ההזרקה ליצירת משטח יציב.
חשוב לשמור על צביעת העור במהלך ההזרקה
שלב 3: הזרקה
א שמור על עור מורם. הכנס את המחט לעור.
- אין לגעת באזור הנקי של העור
B דחוף את הבוכנה בלחץ איטי ויציב עד שתחוש או תשמע "קליק". דחוף את כל הדרך פנימה עד שהוא ילחץ.
- חשוב לדחוף כל הדרך עד ה"טאק "כדי להזריק את המינון המלא.
C שחרר את האגודל. לאחר מכן הרחיק את המזרק מהעור שלך
לאחר שחרור הבוכנה, מגן הבטיחות של המזרק הממולא יכסה את מחט ההזרקה בצורה מאובטחת.
- אין להחזיר את מכסה המחט האפור על מזרקים משומשים שטופלו.
שלב 4: סיים
A זרוק את המזרק הממולא המשומש וחומרים אחרים בכלי לסילוק חד.
יש להיפטר מתרופות בהתאם לתקנות המקומיות. שאל את הרוקח כיצד לזרוק תרופות שאינך משתמש בהן יותר. אמצעים אלה יסייעו בהגנה על הסביבה.
שמור את המזרק ומיכל סילוק החדים הרחק מעיני ילדים.
- אין לעשות שימוש חוזר במזרק הממולא.
- אין למחזר מזרקים מלאים או להשליך אותם לפסולת ביתית.
ב בחן את מקום ההזרקה.
אם אתה מבחין בדם, לחץ על צמר גפן או גזה מעל אתר ההזרקה. אין לשפשף את אתר ההזרקה. במידת הצורך, מרחי תיקון.
הוראות הזרקת פרוליה באמצעות מזרק מלא
חלק זה מכיל מידע על אופן השימוש במזרק הממולא Prolia. חשוב שאתה או המטפל שלך לא תזריקו לפני שקיבלתם הוראות מתאימות מהרופא או מהאחות. שטפו את הידיים לפני כל זריקה. אם יש לכם שאלות בנוגע לזריקה, פנו לרופא או לאחות. צוות סיעודי לקבל עזרה.
לפני שנתחיל
קרא בעיון את כל ההוראות לפני השימוש במזרק הממולא.
אין להשתמש במזרק הממולא אם מכסה המחט הוסר.
כיצד משתמשים במזרק הממולא Prolia מראש?
הרופא שלך רשם מזרק מלא להזרקת פרוליה מתחת לעור (תת עורי). עליך להזריק את כל התכולה (1 מ"ל) של המזרק הממולא Prolia, אותו יש להזריק אחת לשישה חודשים בהתאם להוראות הרופא.
מה שצריך:
כדי לתת לעצמך את הזריקה, תזדקק ל:
- מזרק חדש של Prolia מלא מראש; וכן
- כדורי כותנה ספוגים באלכוהול או חומרי חיטוי דומים.
מה עליך לעשות לפני ההזרקה התת עורית של פרוליה
- הוציאו את המזרק הממולא מהמקרר. אין להרים את המזרק הממולא ליד הבוכנה או בצד המכסה של המחט, שכן הדבר עלול לפגוע בו.
- השאר את המזרק הממולא מחוץ למקרר עד שהוא מגיע לטמפרטורת החדר. זה יהפוך את ההזרקה לנוחה יותר. אין לחמם את המזרק בדרך אחרת (למשל במיקרוגל או במים חמים) אין לחשוף את המזרק לאור שמש ישיר.
- אין לנער את המזרק הממולא יתר על המידה.
- אין להסיר את מכסה המחט מהמזרק הממולא עד שמוכנים להזריק.
- בדוק את תאריך התפוגה על תווית המזרק הממולא (EXP). אין להשתמש בו אם זה לאחר היום האחרון של החודש המוצג.
- בדוק את המראה של פרוליה. זה חייב להיות נוזל צלול, חסר צבע עד צהוב מעט. אין להזריק את הפתרון אם הוא מכיל חלקיקים או אם הוא נראה עכור או דהוי.
- מצאו משטח נוח, מואר ונקי ושמור את כל מה שאתה צריך בהישג יד.
- שטפו את הידיים ביסודיות.
היכן להזריק?
המקומות המתאימים ביותר להזרקה הם הירכיים העליונות והבטן.
אם מישהו שעוזר לך להזריק לך, הוא יכול גם להשתמש בזרוע העליונה החיצונית.
כיצד להזריק?
- לחטא את העור בעזרת מגבון אלכוהול.
- כדי להימנע מכפיפת המחט, משוך בעדינות את המכסה מהמחט בצורה אופקית מבלי לסובב אותה. אין לגעת במחט או לדחוף את הבוכנה.
- אתה עשוי להבחין בבועת אוויר קטנה במזרק הממולא. אסור להסיר את בועת האוויר לפני ההזרקה. הזרקת התמיסה עם בועת האוויר אינה מזיקה.
- הרם את העור בין האגודל לאצבע (בלי לסחוט אותו). דחוף את המחט לגמרי לתוך העור שלך כפי שמוצג על ידי הרופא או האחות שלך.
- דחוף את הבוכנה בלחץ איטי ויציב, ותמיד תשמור על העור. דחוף את הבוכנה עד הסוף עד להזרקת כל הפתרון.
- משוך את המחט ושחרר את העור.
- אם אתה מבחין בטיפת דם, אתה יכול להסיר אותו בעדינות בעזרת צמר גפן או גזה. אין לשפשף את אתר ההזרקה. במידת הצורך, אתה יכול לכסות את אתר ההזרקה בעזרת תיקון
- השתמש בכל מזרק מלא לזריקה אחת בלבד. אין לעשות שימוש חוזר בפרוליה שנותרה במזרק.
זכור: אם יש לך בעיות, אל תהסס להתייעץ עם הרופא או האחות שלך לקבלת עזרה או ייעוץ.
סילוק מזרקים משומשים
- אין להחזיר את המכסה למחטים משומשות.
- שמור מזרקים משומשים הרחק מהישג ידם של ילדים.
- יש להיפטר ממזרקים משומשים בהתאם לדרישות המקומיות. שאל את הרוקח כיצד לזרוק תרופות שאינך משתמש בהן יותר. זה יעזור להגן על הסביבה.
עלון המקור: AIFA (סוכנות התרופות האיטלקית). תוכן שפורסם בינואר 2016. ייתכן שהמידע הנוכחי אינו מעודכן.
כדי לקבל גישה לגרסה העדכנית ביותר, מומלץ לגשת לאתר AIFA (סוכנות התרופות האיטלקית). כתב ויתור ומידע שימושי.
01.0 שם התרופה
פתרון PROLIA 60 MG להזרקה במזרק טרום מילוי
02.0 הרכב איכותי וכמותי
כל מזרק מלא מכיל 60 מ"ג של denosumab ב 1 מ"ל של תמיסה (60 מ"ג / מ"ל).
Denosumab הוא נוגדן חד שבטי אנושי מסוג IgG2 המיוצר בשורת תאים של יונקים (CHO) על ידי טכנולוגיית DNA רקומביננטי.
חומר עזר בעל השפעה ידועה:
כל מ"ל של תמיסה מכיל 47 מ"ג סורביטול (E420) (ראה סעיף 4.4).
לרשימת החומרים המלאים, ראה סעיף 6.1.
03.0 טופס פרמצבטי
פתרון להזרקה (הזרקה).
פתרון שקוף, חסר צבע עד צהוב מעט.
04.0 מידע קליני
04.1 אינדיקציות טיפוליות
טיפול באוסטיאופורוזיס בנשים לאחר גיל המעבר ובגברים בסיכון מוגבר לשברים.
בנשים לאחר גיל המעבר, פרוליה מפחיתה באופן משמעותי את הסיכון לשברים בחוליות, בחוליות ובירך.
טיפול באובדן עצמות הקשור לטיפול הורמונלי אבלטיבי בגברים עם סרטן ערמונית בסיכון מוגבר לשברים (ראה סעיף 5.1). אצל גברים הסובלים מסרטן הערמונית המטופלים בטיפול הורמונלי אבלטיבי, פרוליה מפחיתה באופן משמעותי את הסיכון לשברים בחוליות.
04.2 מינון ושיטת הניהול
מִנוּן
המינון המומלץ של פרוליה הוא 60 מ"ג הניתן בזריקה תת עורית אחת ל 6 חודשים בירך, בבטן או בזרוע העליונה.
על המטופלים לקבל תוספת מספקת של סידן וויטמין D (ראה סעיף 4.4).
לחולים המטופלים בפרוליה יש לתת את העלון וכרטיס התזכורת למטופל.
חולים עם ליקוי כלייתי
אין צורך בהתאמת מינון בחולים עם ליקוי בכליות (ראה סעיף 4.4 להמלצות על ניטור סידן).
חולים עם ליקוי בכבד
הבטיחות והיעילות של denosumab לא נחקרו בחולים עם ליקוי בכבד (ראה סעיף 5.2).
חולים קשישים (גיל ≥ 65)
אין צורך בהתאמת מינון בחולים קשישים.
אוכלוסיית ילדים
פרוליה אינה מומלצת בחולי ילדים (גיל
שיטת ניהול
לשימוש תת עורי.
הניהול צריך להתבצע על ידי אדם שהוכשר כטכניקות הזרקה.
להוראות שימוש, טיפול וסילוק, ראה סעיף 6.6.
04.3 התוויות נגד
• היפוקלצמיה (ראה סעיף 4.4).
• רגישות יתר לחומר הפעיל או לכל אחד מהחומרים המצוינים בסעיף 6.1.
04.4 אזהרות מיוחדות ואמצעי זהירות מתאימים לשימוש
צריכת סידן וויטמין D.
חשוב שכל החולים יקבלו כמות מספקת של סידן וויטמין D.
אמצעי זהירות לשימוש
היפוקלצמיה
חשוב לזהות חולים בסיכון להיפוקלצמיה.יש לתקן היפוקלצמיה על ידי צריכת סידן וויטמין D נאותה לפני תחילת הטיפול. מומלץ לבצע ניטור קליני של רמות הסידן לפני כל מנה ובחולים המועדים להתפתחות היפוקלצמיה תוך שבועיים מהמינון. אם חלק מהחולים חווים סימפטומים חשודים של היפוקלקמיה במהלך הטיפול (ראה סעיף 4.8 לרשימת התסמינים) יש למדוד את רמות הסידן. יש לעודד את החולים לדווח על תסמינים המעידים על היפוקלצמיה.
דיווחו על היפוקלצמיה סימפטומטית חמורה במסגרת השיווק שלאחר השיווק (ראה סעיף 4.8) שהתרחשו במרבית המקרים בשבועות הראשונים לאחר תחילת הטיפול, אך אשר עשויים להתרחש גם מאוחר יותר.
זיהומים בעור
חולים המטופלים בפרוליה עלולים לפתח דלקות עור (בעיקר צלוליטיס) הדורשות אשפוז (ראה סעיף 4.8). יש לומר לחולים לפנות לטיפול רפואי מיידי אם הם מפתחים סימנים או תסמינים של צלוליטיס.
אוסטאונקרוזיס של הלסת (ONJ)
ONJ דווחה לעיתים נדירות בחולים שטופלו ב- Prolia לטיפול באוסטאופורוזיס (ראה סעיף 4.8).
יש לדחות את תחילת הטיפול / טיפול חדש בחולים עם נגעים שאינם מרפאים, פתוחים ורקמים רכים בפה. בדיקת שיניים עם מניעת שיניים והערכת תועלת / סיכון פרטנית מומלצת לפני טיפול בפרוליה בחולים. עם גורמי סיכון נלווים.
יש לקחת בחשבון את גורמי הסיכון הבאים בעת הערכת הסיכון של המטופל לפתח ONJ:
• עוצמת התרופה המעכבת את ספיגת העצם (הסיכון גבוה יותר עם תרופות חזקות יותר), דרך הניהול (הסיכון גבוה יותר במתן פרנטרלי) והמינון המצטבר של טיפול בספיגת עצם.
• גידול, מצבים חולניים (למשל אנמיה, קרישת דם, זיהום), עישון.
• טיפולים מקבילים: סטרואידים, כימותרפיה, מעכבי אנגיוגנזה, הקרנות באזור הראש והצוואר.
• היגיינת פה לקויה, מחלת חניכיים, תותבות שיניים שהוכנסו בצורה לא נכונה, מחלת שיניים קיימת, הליכי שיניים פולשניים כגון עקירות שיניים.
יש לעודד את כל המטופלים לשמור על היגיינת הפה, לבצע בדיקות שיניים סדירות ולדווח באופן מיידי על כל תסמינים אוראליים כגון ניידות שיניים, כאבים או נפיחות או אי החלמה של פצעים בפה או הימצאות הפרשות במהלך הטיפול. טיפול בפרוליה. במהלך הטיפול, יש לבצע הליכי שיניים פולשניים רק לאחר בחינה מדוקדקת ויש להימנע מהם בסמיכות למינהל פרוליה.
יש להגדיר את תוכנית הניהול לחולים המפתחים ONJ בשיתוף פעולה הדוק בין הרופא המטפל לרופא שיניים או מנתח פה בעל ניסיון עם ONJ. יש לשקול הפסקת טיפול זמנית עד לפתרון המצב ובמידת האפשר, להקל על גורמי הסיכון. שתרם להתרחשותו.
שברים לא טיפוסיים של עצם הירך
מקרים של שברים ירך לא טיפוסיים דווחו בחולים שטופלו בפרוליה (ראה סעיף 4.8). שברים ירך לא טיפוסיים יכולים להתרחש עם טראומה מינימלית או ללא טראומה באזורים התחתוניים והדיאפיזאליים של עצם הירך. אירועים אלה מאופיינים בממצאים רדיוגרפיים ספציפיים. כמו כן דווח על שברים בירך לא טיפוסית
הוא בחולים עם כמה מחלות נלוות (למשל מחסור בוויטמין D, דלקת מפרקים שגרונית, היפופוספטסיה) ובמקרה של שימוש בתרופות מסוימות (למשל ביספוספונטים, גלוקוקורטיקואידים, מעכבי משאבת פרוטון). אירועים אלה התרחשו גם בהיעדר טיפול אנטי ספיגה. שברים דומים, המדווחים בקשר עם שימוש בביספוספונטים, הם לרוב דו-צדדיים; לכן יש להעריך את עצם הירך הנגדית בחולים שטופלו בפרוליה שסבלו משבר פיר הירך. בחולים עם חשד לשבר ירך לא טיפוסי, יש לשקול L. של טיפול בפרוליה, בהמתנה להערכת המטופל המבוססת על ניתוח תועלת / סיכון אישי. במהלך הטיפול בפרוליה, יש לייעץ למטופלים לדווח על כאבים חדשים או יוצאי דופן בירך, בירך או במפשעה. יש להעריך את המטופלים המופיעים בתסמינים כאלה לשבר ירך שלם.
טיפול במקביל עם תרופות אחרות המכילות denosumab
אין לטפל בחולים המטופלים בפרוליה במקביל לתרופות אחרות המכילות denosumab (למניעת אירועי שלד אצל מבוגרים עם גרורות בעצמות מגידולים מוצקים).
ליקוי כלייתי
חולים עם ליקוי כלייתי חמור (דיאליזה של קריאטינין בסיכון מוגברת לפתח היפוקלצמיה. הסיכון לפתח היפוקלצמיה וכתוצאה מכך עלייה ברמות ההורמון הפאראתירואיד עולה עם עלייה ברמת הכליות. צריכת סידן מספקת, ויטמין D וניטור סידן קבוע חשובים במיוחד. בחולים אלה, כפי שצוין לעיל.
גומי טבעי יבש
מכסה המחט של המזרק הממולא מכיל גומי טבעי יבש (נגזרת של לטקס), שעלול לגרום לתגובות אלרגיות.
אזהרות עבור חומרי עזר
תרופה זו מכילה סורביטול. חולים עם מצבים תורשתיים נדירים של אי סבילות לפרוקטוז לא צריכים לקחת פרוליה.
תרופה זו מכילה פחות מ- 1 mmol נתרן (23 מ"ג) ל -60 מ"ג, כלומר "ללא נתרן".
04.5 אינטראקציות עם מוצרי תרופות אחרים וצורות אינטראקציה אחרות
במחקר אינטראקציה, פרוליה לא השפיעה על הפרמקוקינטיקה של midazolam, שעוברת מטבוליזם על ידי ציטוכרום P450 3A4 (CYP3A4). זה מצביע על כך ש- Prolia לא צפויה לשנות את הפרמקוקינטיקה של מוצרים רפואיים שעוברים מטבוליזם על ידי CYP3A4.
אין נתונים קליניים זמינים לגבי מתן טיפול מקביל של denosumab וטיפול הורמונאלי חלופי (אסטרוגן), אולם סיכון פוטנציאלי לאינטראקציה פרמקודינמית נחשב נמוך.
במחקר קליני מעבר (alendronate ל- denosumab) בנשים לאחר גיל המעבר עם אוסטאופורוזיס, הפרמקוקינטיקה והפרמקודינמיקה של denosumab לא שונו על ידי טיפול קודם באלנדרונאט.
04.6 הריון והנקה
הֵרָיוֹן
אין נתונים מספקים לגבי השימוש בפרוליה בנשים בהריון.הוכחה רעילות הרבייה במחקר שנערך על קופי צינומולגוס שטופלו במהלך ההריון במינוני דנוסומאב וכתוצאה מכך חשיפה מערכתית פי 119 במונחים של AUC. גבוהה מהמינון המשמש בבני אדם. (ראה סעיף 5.3).
השימוש בפרוליה אינו מומלץ לנשים בהריון.
נשים שנכנסות להריון בזמן שהן מטופלות בפרוליה מעודדות להירשם לתכנית מעקב ההריון של אמגן. פרטי יצירת הקשר ניתנים בסעיף 6 בעלון החבילה - מידע למשתמש.
זמן האכלה
לא ידוע אם denosumab מופרש בחלב אם. מחקרים שנערכו בעכברים מהונדסים גנטית שבהם הגן המקודד ל- RANKL הוסר (עכברי נוקאאוט) מצביעים על כך שהיעדר RANKL (היעד של denosumab - ראה סעיף 5.1) במהלך ההריון עלול להפריע להבשלה של בלוטת החלב. בהנקה לאחר הלידה (ראה סעיף 5.3). יש לקבל החלטה אם להימנע מהנקה או מטיפול בפרוליה, תוך התחשבות בתועלת ההנקה עבור התינוק / תינוק ויתרון הטיפול בפרוליה לאישה.
נשים מיניקות במהלך הטיפול בפרוליה מעודדות להירשם לתכנית מעקב ההנקה של אמגן. פרטי התקשרות מופיעים בסעיף 6 בעלון החבילה - מידע למשתמש.
פוריות
אין נתונים על ההשפעות של denosumab על פוריות האדם. מחקרים בבעלי חיים אינם מצביעים על השפעות מזיקות ישירות או עקיפות על הפוריות (ראה סעיף 5.3).
04.7 השפעות על יכולת הנהיגה וההתנהלות במכונות
לפרוליה אין השפעה או זניחה על יכולת הנהיגה או השימוש במכונות.
04.8 תופעות לא רצויות
סיכום פרופיל הבטיחות
פרופיל הבטיחות הכולל של Prolia היה דומה בחולים עם אוסטאופורוזיס ובחולים עם סרטן שד או ערמונית שטופלו בטיפול אבלטיבי הורמונלי בחמישה ניסויים קליניים שלב III מבוקרי פלסבו.
תופעות הלוואי השכיחות ביותר של Prolia (הנצפות ביותר מאחד מכל עשרה חולים) הן כאבי שריר ושלד וכאבים בגפיים. מקרים של צלוליטיס נצפו באופן נדיר בחולים שטופלו בפרוליה; מקרים נדירים של היפוקלצמיה, רגישות יתר, אוסטאונקרוזיס של הלסת ושברים ירךיים לא טיפוסיים (ראה סעיף 4.4 וסעיף 4.8 - תיאור תגובות שליליות נבחרות).
טבלה של תגובות שליליות
הנתונים המוצגים בטבלה 1 מתארים תופעות לוואי שדווחו בניסויים קליניים שלב II ו- III בחולים עם אוסטאופורוזיס ובחולים עם סרטן שד או ערמונית שקיבלו טיפול הורמונלי אבלטיבי ו / או מדיווחים ספונטניים.
האמנה הבאה שימשה לסיווג תגובות שליליות (ראו טבלה 1): שכיחה מאוד (1/10 ≥), שכיחה (≥ 1/100,
טבלה 1 תגובות שליליות שדווחו בחולים עם אוסטיאופורוזיס וחולי סרטן השד או הערמונית שטופלו בטיפול הורמונלי אבלטיבי
1 ראה סעיף תיאור תגובות שליליות שנבחרו
בניתוח מאוחד של הנתונים מכל הניסויים הקליניים שלב II ו- III מבוקרי פלסבו, דווח על תסמונת דמוית שפעת עם שיעור שכיחות גולמי של 1.2% בנבדקים שטופלו ב- denosumab ו -0.7% בנבדקים שטופלו בפלסבו. למרות שהבדל זה צץ ב "ניתוח משולב של המחקרים השונים, הוא לא נצפה בניתוח" מרובד.
תיאור תגובות שליליות נבחרות
היפוקלצמיה
בשני ניסויים קליניים שלב III מבוקרי פלסבו בנשים עם אוסטאופורוזיס לאחר גיל המעבר, כ -0.05% (2 מתוך 4,050) מהחולים דיווחו על ירידה ברמות הסידן בסרום (פחות מ -1.88 ממול / ליטר) לאחר מתן פרוליה. מאידך גיסא, ירידות ברמות הסידן בסרום (פחות מ -1.88 ממול / ליטר) לא דווחו בשני הניסויים הקליניים מבוקרי פלסבו שלב III בחולים שטופלו בטיפול אובליסטי הורמונלי או בניסוי קליני מבוקר פלסבו שלב III ב גברים עם אוסטאופורוזיס.
במסגרת השיווק, דווח על מקרים נדירים של היפוקלצמיה חמורה סימפטומטית בעיקר בחולים שטופלו בפרוליה בסיכון מוגבר להיפוקלצמיה, שהתרחשו במרבית המקרים בשבועות הראשונים לאחר תחילת הטיפול. דוגמאות לביטויים קליניים של היפוקלצמיה סימפטומטית חמורה, כולל הארכת מרווח QT, טטניה, התקפים ושינוי מצב נפשי (ראה סעיף 4.4). סימפטומים של היפוקלצמיה בניסויים קליניים עם denosumab כללו חוסר תחושה או נוקשות בשרירים, עוויתות שרירים, עוויתות והתכווצויות.
זיהומים בעור
בניסויים קליניים שלב III מבוקרי פלסבו בנשים עם אוסטאופורוזיס לאחר גיל המעבר, השכיחות הכוללת של דלקות עור הייתה דומה בקבוצות הפלסבו והפרוליה (פלסבו [1.2%, 50 מתוך 4,041] לעומת פרוליה [1.5%, 59 מתוך 4,050] ); אצל גברים עם אוסטאופורוזיס (פלצבו [0.8%, 1 מתוך 120] לעומת פרוליה [0%, 0 מתוך 120]. עדויות דומות נצפו גם במחקרים קליניים שלב III בניסויים מבוקרי פלסבו בחולי סרטן השד או סרטן הערמונית שטופלו ב- טיפול אבלטיבי הורמונלי (פלצבו [1.7%, 14 מתוך 845] לעומת פרוליה [1.4%, 12 מתוך 860]). שנדרשו אשפוז דווחו אצל 0.1%(3 מתוך 4,041) מהנשים עם אוסטאופורוזיס לאחר גיל המעבר שטופלו בפלסבו, לעומת 0.4% (16 מתוך 4,050) מהנשים שקיבלו פרוליה. לרוב אלו היו מקרים של צלוליטיס במחקרים שנערכו על חולים עם סרטן השד והערמונית, l ודלקות עור שדווחו כתופעות לוואי חמורות היו דומות בקבוצות הפלסבו (0.6%, 5 מתוך 845) ובפרוליה (0.6%, 5 מתוך 860).
אוסטאונקרוזיס של הלסת התחתונה / מקסימה
בניסויים קליניים באוסטיאופורוזיס ובחולי סרטן השד או הערמונית שקיבלו טיפול אובליטיבי הורמונלי בסך הכל 19,521 חולים ONJ דווחה לעיתים רחוקות אצל 14 חולים (ראה סעיף 4.4).
שברים לא טיפוסיים של עצם הירך
בתוכנית ההתפתחות הקלינית של אוסטאופורוזיס, דיווחו לעתים רחוקות על שברים בירך הירך בחולים שטופלו בפרוליה (ראה סעיף 4.4).
קָטָרַקט
בניסוי קליני שלב III בודד מבוקר פלסבו בחולי סרטן הערמונית שקיבלו טיפול במניעת אנדרוגן (ADT), נצפה הבדל בשכיחות קטרקט (4.7% דנוסומב, 1.2% פלסבו). לא נצפה הבדל בנשים עם אוסטאופורוזיס לאחר גיל המעבר. או אצל גברים הסובלים מאוסטיאופורוזיס או בנשים שטופלו במעכבי ארומטאז לסרטן שד לא גרורתי.
דיברטיקוליטיס
הבדל בשכיחות דיברטיקוליטיס (1.2% דנוסומאב, 0% פלסבו) נצפה בניסוי קליני מבוקר פלסבו שלב III בחולי סרטן הערמונית שקיבלו טיפול בחוסר אנדרוגן (ADT). L שכיחות דיברטיקוליטיס הייתה דומה בין קבוצות טיפול בנשים עם אוסטאופורוזיס לאחר גיל המעבר או בגברים הסובלים מאוסטיאופורוזיס ובנשים שטופלו במעכבי ארומטאז לסרטן שד לא גרורתי.
תגובות רגישות יתר לתרופה
אירועים נדירים של רגישות יתר לתרופה, כולל פריחה, אורטיקריה, נפיחות בפנים, אריתמה ותגובות אנפילקטיות דווחו בדיווחים לאחר השיווק בחולים שקיבלו פרוליה.
כאבי שרירים ושלד
כאבים בשרירים ושלד, כולל מקרים חמורים, דווחו בחולים שטופלו בפרוליה במסגרת השיווק שלאחר השיווק. בניסויים קליניים כאבי שרירים ושלד היו נפוצים מאוד הן בקבוצות הדנוסומאב והן בקבוצת הפלצבו. כאבי שרירים ושלד שהביאו.
אוכלוסיות מיוחדות אחרות
בניסויים קליניים, חולים עם ליקוי כלייתי חמור (פינוי קריאטינין
דיווח על חשדות לתגובות שליליות
חשוב לדווח על תגובות שליליות החשודות המתרחשות לאחר אישור המוצר, שכן הוא מאפשר מעקב רציף אחר איזון התועלת / סיכון של המוצר. אנשי מקצוע בתחום הבריאות מתבקשים לדווח על כל חשד לתגובות שליליות באמצעות מערכת הדיווח הלאומית (רשות התרופות האיטלקית - אתר אינטרנט: https://www.aifa.gov.it/content/segnalazioni-reazioni-avverse).
04.9 מנת יתר
לא דווח על מקרים של מנת יתר במחקרים קליניים. בניסויים קליניים ניתנה denosumab במינונים של עד 180 מ"ג כל 4 שבועות (מינונים מצטברים עד 1,080 מ"ג במשך 6 חודשים) ולא נצפו תגובות שליליות נוספות.
05.0 נכסים פרמקולוגיים
05.1 תכונות פרמקודינמיות
קבוצה פרמקותרפית: תרופות לטיפול במחלות עצם - תרופות אחרות המשפיעות על מבנה העצם ומינרליזציה, קוד ATC: M05BX04
מנגנון הפעולה
Denosumab הוא נוגדן חד -שבטי אנושי (IgG2) המופנה כנגד RANKL, אליו הוא נקשר בזיקה וספציפיות גבוהה, ומונע את הפעלת קולטן ה- RANK שלו, הנמצא על פני השטח של האוסטאוקלסטים ומקדמיהם. חסימת האינטראקציה בין RANKL ל- RANK מעכבת את היווצרותם, תפקודם והישרדותם של אוסטאוקלאסטים, ובכך מפחיתים את ספיגת העצם, הן ברמת הקליפת המוח והן ברמה הטרבקולרית.
השפעות פרמקודינמיות
טיפול בפרוליה הפחית במהירות את מחזור העצמות והגיע לסף הסרום של ספיגת העצם C- מסוף טלופפטיד קולגן מסוג I (CTX) (הפחתה של 85%) תוך 3 ימים. נשמר לאורך כל מרווח המינון. בסוף כל מרווח מינון, הירידות ב- CTX נחלשו באופן חלקי מירידה מקסימלית של ≥ 87% לכ- 45% בערך (טווח 45-80%), המשקפות את הפיכות ההשפעות של פרוליה על שיפוץ העצמות לאחר ירידה ברמות הסרום. השפעות אלה נשמרו על ידי המשך הטיפול בפרוליה. סמנים של מחזור העצמות הגיעו בדרך כלל לרמות שלפני הטיפול תוך 9 חודשים מהמינון האחרון. עם חידוש הטיפול, הפחתות הנגרמות על ידי denosumab ב- CTX היו דומות לאלה שנראו בחולים נאיבים שהתחילו בטיפול ב- denosumab.
אימונוגניות
במחקרים קליניים לא נצפו נוגדנים מנטרלים המכוונים נגד פרוליה. בהתבסס על תוצאות בדיקה חיסונית רגישה, פחות מ -1% מהחולים שטופלו ב- denosumab עד 5 שנים נבדקו חיוביים לגבי נוגדנים לא מנטרלים ללא עדות לשינוי בפרופיל התגובה הפרמקוקינטית, הטוקסיקולוגית או הקלינית.
טיפול באוסטאופורוזיס לאחר גיל המעבר
היעילות והבטיחות של Prolia הניתנים כל 6 חודשים למשך 3 שנים הוערכו בקרב נשים לאחר גיל המעבר (7,808 נשים בגילאי 60 עד 91 שנים מתוכן 23.6% היו עם שברים חוליות שכיחות) עם ערכים בסיסיים BMD (צפיפות מינרלים בעצמות) המתבטאים בעמוד השדרה המותני או סך כל ציוני T עצם הירך הנעים בין -2.5 ל -4.0 ועם הסתברות מוחלטת לשבר של 10 שנים לשברים של 18.60% (עשירונים: 7.9-32.4%) לשברים אוסטאופורוטיים גדולים ו -7.22% (עשירונים: 1.4-14.9%) עבור שברים בירך. המשפיעים על חילוף החומרים בעצמות לא נכללו במחקר. המטופלים קיבלו תוסף סידן יומי (לפחות 1,000 מ"ג) וויטמין D (לפחות 400 IU).
השפעות על שברים בחוליות
פרוליה הפחיתה באופן משמעותי את הסיכון לשברים חדשים בחוליות בגיל 1, 2 ו -3 שנים (עמ
טבלה 2 השפעות פרוליה על הסיכון לשברים חדשים בחוליות
* עמ '
השפעות על שברים בירך
פרוליה הוכיחה הפחתה יחסית של 40% (הפחתת סיכון מוחלטת של 0.5%) בסיכון לשלוש שנים לשברים בירך (עמ
בניתוח פוסט-הוק בקרב נשים מעל גיל 75, Prolia הראתה הפחתת סיכון יחסית של 62% (הפחתת סיכון מוחלטת של 1.4%, p
השפעות על כל השברים הקליניים
פרוליה הפחית באופן משמעותי את כל סוגי השברים / קבוצות (ראה טבלה 3).
טבלה 3 השפעות פרוליה על הסיכון לשברים קליניים ל -3 שנים
* p ≤ 0.05; ** p = 0.0106 (נקודת קצה משנית לאחר תיקון ריבוי), *** p ≤ 0.0001
+ שכיחות אירועים המבוססת על הערכות של קפלן-מאייר לשלוש שנים.
1 כולל שברים חוליות וחוליות קליניות.
2 לא כולל אלה המשפיעים על החוליות, הגולגולת, הפנים, הלסת התחתונה, המטקרפוס והפלנגות של האצבעות והבהונות.
3 כולל אגן, עצם עצם דיסטלית, עצם שוקה פרוקסימלית, צלעות, עצם עצם פרוקסימלית, אמה ועצם הירך.
4 כולל שברי חוליות, עצם הירך, האמה והזרוע, כפי שהוגדר על ידי ארגון הבריאות העולמי.
בנשים עם ערכי BMD בסיסיים המתבטאים בצוואר הירך T- ציון ≤ -2.5 פרוליה הפחית את הסיכון לשברים לא חוליות (הפחתת סיכון יחסי של 35%, הפחתת סיכון מוחלטת של 4.1%, p
הירידה של שלוש שנים בפרוליה בשכיחות שברים חדשים בחוליות, שברים בירך ושברים שאינם חוליות נותרה קבועה, ללא קשר לסיכון לשבר בסיסי לאחר 10 שנים.
השפעות על צפיפות מינרלים בעצמות
בהשוואה לטיפול פלסבו, פרוליה הגדילה באופן משמעותי את ה- BMD בכל אתרי השלד הנמדדים בגיל שנה, שנתיים ו -3. פרוליה הגדילה את ה- BMD ב -9.2% בעמוד השדרה המותני, ב -6.0% בכל עצם הירך, ב -4.8% בצוואר הירך, ב -7.9% בטרונטר, ב -3, 5% ברמה של השליש הרחוק של הרדיוס. ו -4.1% ברמת הגוף הכולל במשך 3 שנים (כל עמ '
בניסויים קליניים שהעריכו את ההשפעות של הפסקת Prolia, BMD חזר לרמות שלפני הטיפול לפני 18 חודשים מהמינון האחרון ונשאר מעל פלסבו. נתונים אלה מצביעים על כך שהמשך הטיפול בפרוליה נחוץ כדי לשמור על השפעת הטיפול. חידוש הטיפול בפרוליה הביא לעלייה ב- BMD הדומה לאלה שנראו כאשר פרוליה ניתנה לראשונה.
מחקר הרחבה בעל תווית פתוחה לטיפול באוסטאופורוזיס לאחר גיל המעבר
בסך הכל 4,550 נשים (2,343 פרוליה ו -2,207 פלסבו) שלא פספסו יותר ממתן תרופות אחד במחקר המרכזי שתואר לעיל ושסיימו את הביקור בחודש 36 של המחקר, נתנו הסכמה להירשם למחקר של רב לאומי, הארכת מרכזית, פתוחה, חד זרוע, הנמשכת 7 שנים להערכת הבטיחות והיעילות לטווח הארוך של פרוליה. כל הנשים במחקר ההרחבה קיבלו את פרוליה במינון של 60 מ"ג כל 6 חודשים, וכן קיבלו סידן יומי ( לפחות 1 גרם) וויטמין D (לפחות 400 IU). בחודש 60 של מחקר ההרחבה, לאחר 8 שנים של טיפול בפרוליה, בקבוצה ארוכת הטווח (n = 1,542) ה- BMD עלה ב- 18, 4% בעמוד השדרה המותני, 8.3% בכל עצם הירך, 7.8% בצוואר הירך ו -11.6% בטרונטר מההתחלה במחקר המרכזי המקורי.
שכיחות השברים הוערכה כנקודת קצה בטיחותית.
מהשנה הרביעית עד השמונה שכיחותם של שברים חדשים בחוליות ולא בחוליות לא עלתה עם הזמן; השכיחות על בסיס שנתי הייתה כ -1.1% ו -1.3% בהתאמה.
שמונה מקרים מאושרים של אוסטאונקרוזיס של הלסת (ONJ) ושני שברים לא טיפוסיים של עצם הירך התרחשו במהלך מחקר ההרחבה.
טיפול באוסטיאופורוזיס אצל גברים
היעילות והבטיחות של Prolia, הניתנים פעם בחצי שנה למשך שנה אחת, הוערכו בקרב 242 גברים בגילאי 31 עד 84 שנים. נבדקים עם שיעור סינון גלומרולרי משוער (eGFR) 2 היו כל הגברים שקיבלו סידן יומי (לפחות 1,000 מ"ג). ותוסף ויטמין D (לפחות 800 IU).
משתנה היעילות העיקרי היה השינוי באחוזים ב- BMD בעמוד השדרה המותני; היעילות נגד שברים לא הוערכה. פרוליה הגדילה באופן משמעותי את ה- BMD בכל אתרי השלד שנמדדו בהשוואה לפלסבו בגיל 12 חודשים: 4.8% בעמוד השדרה המותני, 2.0% בכל עצם הירך, 2.2% ברמת צוואר הירך, 2.3% ברמת הצוואר הירך. רמת הטרונטר, ו -0.9% ברמה של השליש הדיסטלי של הרדיוס (כל עמ '
היסטולוגיה של עצמות
היסטולוגית העצמות הוערכה לאחר 1-3 שנים של טיפול בפרוליה ב -62 נשים עם אוסטאופורוזיס לאחר גיל המעבר או מסת עצם נמוכה שלא קיבלו טיפול באוסטיאופורוזיס או שטופלו בעבר באלנדרונט. 41 נשים השתתפו בתת-מחקר ביופסיה של עצמות בחודש 24 למחקר ההרחבה. היסטולוגיה של העצמות הוערכה גם בקרב 17 גברים עם אוסטאופורוזיס לאחר שנה של טיפול בפרוליה. תוצאות ביופסיה של עצמות הראו עצם של ארכיטקטורה ואיכות נורמלית ללא עדות לפגמים מינרליזציה, עצם לא-מללרית או פיברוזיס מדולרי.
טיפול באובדן עצמות הקשור בטיפול בחסך אנדרוגן
היעילות והבטיחות של פרוליה, הניתנת אחת ל -6 חודשים למשך 3 שנים, הוערכו בגברים עם סרטן ערמונית שאינו גרורתי שאינו גרורתי שטופלו ב- ADT (1,468 גברים בגילאי 48 עד 97 שנים) עם סיכון מוגבר לשברים (מוגדר כגיל > 70 שנה או
בהשוואה לטיפול פלסבו, פרוליה הגדילה באופן משמעותי את ה- BMD בכל אתרי השלד הנמדדים ב -3 שנים ב -7.9% ברמת עמוד השדרה המותני, ב -5.7% ברמת עצם הירך הכוללת, ב -4.9% בצוואר הירך, 6.9% ברמת הטרונטר, 6.9% בשליש הרחוק של הרדיוס ו -4.7% ברמת הגוף הכוללת (כל עמ '
פרוליה הוכיחה ירידה משמעותית בסיכון היחסי לשברים חדשים בחוליות: 85% (הפחתת סיכון מוחלטת של 1.6%) בשנה אחת, 69% (הפחתת סיכון מוחלטת של 2.2%) לאחר שנתיים ו- 62% (הפחתת סיכון מוחלטת של 2.4% ) בגיל 3 שנים (כל עמ '
טיפול באובדן עצם הקשור לטיפול במעכבי ארומטאז משלים
היעילות והבטיחות של Prolia הניתנים אחת לשישה חודשים למשך שנתיים הוערכו בנשים עם סרטן שד לא גרורתי (252 נשים בגילאי 35 עד 84 שנים) עם ערכי BMD בסיסיים המתבטאות בציוני T. החל מ -1.0 עד -2.5 ברמה של עמוד השדרה המותני, סך עצם הירך או צוואר הירך. כל הנשים קיבלו תוספת יומית של סידן (לפחות 1,000 מ"ג) וויטמין D (לפחות 400 IU).
נקודת סיום היעילות העיקרית של המחקר הייתה שינוי באחוזים ב- BMD בעמוד השדרה המותני, בעוד שיעילות השברים לא הוערכה. בהשוואה לטיפול שנתיים בפלסבו, פרוליה הגדילה באופן משמעותי את ה- BMD בכל אתרי השלד הנמדדים של 7.6% ברמה של עמוד השדרה המותני. , 4.7% ברמה של עצם הירך הכוללת, 3.6% ברמת צוואר הירך, 5.9% ברמת הטרוצ'נטר, 6.1% ברמת השליש הדיסטלי של הרדיוס ו -4.2% ברמת הגוף הכוללת. (הכל P
אוכלוסיית ילדים
סוכנות התרופות האירופית ויתרה על החובה למסור את תוצאות המחקרים עם Prolia בכל תת קבוצות האוכלוסייה הילדים לטיפול באובדן עצם הקשור לטיפול הורמונלי אבלטיבי, ובקבוצות משנה של אוכלוסיית הילדים בגיל צעיר יותר. שנתיים עבור טיפול באוסטיאופורוזיס. עיין בסעיף 4.2 למידע על שימוש בילדים.
05.2 תכונות פרמקוקינטיות
קְלִיטָה
לאחר מתן תת עורית של מינון של 1.0 מ"ג / ק"ג, המקביל למינון המאושר של 60 מ"ג, החשיפה המבוססת על AUC הייתה 78% בהשוואה למתן תוך ורידי של אותה מנה. למינון תת עורי של 60 מ"ג, ריכוז הסרום המרבי (Cmax) של denosumab של 6 mcg / ml (טווח 1-17 mcg / ml) הושג תוך 10 ימים (טווח 2-28 ימים).
ביו טרנספורמציה
Denosumab מורכב אך ורק מחומצות אמינו ופחמימות כגון אימונוגלובולינים מקומיים ולא סביר שיבוטלו על ידי חילוף חומרים בכבד. ניתן לצפות לחילוף החומרים ולחיסול התרופה לעקוב אחר מסלולי פינוי אימונוגלובולינים, וכתוצאה מכך להתדרדרות לפפטידים קטנים וחומצות אמינו בודדות.
חיסול
לאחר שהגיע Cmax, רמות הסרום ירדו עם "מחצית חיים של 26 ימים (טווח 6-52 ימים) לאורך תקופה של 3 חודשים (טווח 1.5-4.5 חודשים). ל -53% מהחולים לא הייתה כמות ניתנת למדידה של denosumab תוך 6 חודשים. לאחר מתן מינון.
לא נצפתה הצטברות או שינוי בפרמקוקינטיקה של denosumab לאורך זמן לאחר מינון רב -עורי של 60 מ"ג אחת לשישה חודשים. הפרמקוקינטיקה של דנוסומאב לא הושפעה מהיווצרות נוגדנים המחייבים תרופות והיו דומים בקרב גברים ונשים. גיל (28-87 שנים), גזע ומצב מחלה (ירידה במסת עצם או אוסטיאופורוזיס; סרטן הערמונית או השד) לא נראה שיש להם השפעות משמעותיות על הפרמקוקינטיקה של denosumab.
בהתבסס על AUC ו- Cmax, הייתה מגמה בין משקל גוף גבוה יותר לבין חשיפה נמוכה יותר לתרופות. עם זאת, מגמה זו לא נחשבה רלוונטית מבחינה קלינית, שכן השפעות פרמקודינמיות המבוססות על סמני מחזור עצמות ועליות BMD היו קבועות בטווח רחב של משקל גוף. .
לינאריות / לא ליניאריות
במחקרים הנעים במינונים, denosumab הציגה פרמקוקינטיקה לא לינארית ותלויה במינון, עם פינוי נמוך יותר במינונים או בריכוזים גבוהים יותר, אך עם עלייה בערך במינון החשיפה למינונים שווים או גבוהים יותר עד 60 מ"ג.
ליקוי כלייתי
במחקר שנערך על 55 חולים עם דרגות שונות של תפקוד כלייתי, כולל חולים בדיאליזה, למידת הפגיעה בכליות לא הייתה השפעה על הפרמקוקינטיקה של denosumab.
ספיקת כבד
לא בוצעו מחקרים ספציפיים בחולים עם תפקוד כבד לקוי. באופן כללי, נוגדנים חד שבטיים אינם מסולקים על ידי חילוף חומרים בכבד. הפרמקוקינטיקה של Denosumab צפויה להיות מושפעת מפגיעה בתפקוד הכבד.
אוכלוסיית ילדים
הפרופיל הפרמקוקינטי באוכלוסיית הילדים לא הוערך.
05.3 נתוני בטיחות פרה -קליניים
במחקרי רעילות של מנה אחת וחוזרת שנערכו בקופי צינומולגוס, למינונים של denosumab שהובילו לחשיפה מערכתית עד פי 100-150 מהמינון האנושי המומלץ לא הייתה השפעה על הפיזיולוגיה הקרדיווסקולרית, על פוריות הגבר או על הנקבה.
לא בוצעו בדיקות סטנדרטיות לחקר הגנוטוקסיות הפוטנציאלית של denosumab, שכן בדיקות אלה אינן רלוונטיות למולקולה זו. עם זאת, בהתחשב במאפייניו, לא סביר שיש ל- denosumab פוטנציאל גנוטוקסי.
הפוטנציאל המסרטן של denosumab לא הוערך במחקרים בבעלי חיים ארוכי טווח.
במחקרים פרה -קליניים שנערכו בעכברי נוקאאוט שלא הביעו RANK או RANKL, נצפתה פגיעה ביצירת בלוטות הלימפה העוברית. היעדרות הנקה עקב עיכוב של התבגרות בלוטת החלב (התפתחות המבנים הלובולו-אלוולאריים של הבלוטה במהלך ההריון) נצפתה גם בעכברי נוקאאוט שלא הביעו RANK או RANKL.
במחקר שנערך על קופי צינומולגוס שטופלו במהלך התקופה המקבילה לטרימסטר הראשון להריון עם מינוני דנוסומאב וכתוצאה מכך חשיפה מערכתית מבחינת AUC עד פי 99 מהמינון האנושי (60 מ"ג כל 6 חודשים), ללא פגיעה באם או דווח על העובר. בלוטות לימפה עובריות לא נבדקו במחקר זה.
במחקר אחר בקופי סינומולגוס שטופלו במהלך ההריון במינוני דנוסומאב וכתוצאה מכך חשיפה מערכתית במונחים של AUC פי 119 מהמינון ששימש לבני אדם (60 מ"ג כל 6 חודשים), נצפתה עלייה בעוברים. לידות מת ותמותה לאחר לידה; צמיחת עצם לא תקינה עם ירידה בחוזק העצמות, הפחתת המטופויזיה ויישור שגוי בשיניים; היעדר בלוטות לימפה היקפיות וצמיחה ילודה מופחתת. לא נקבעה רמה שבה לא נצפות השפעות מזיקות על הרבייה. שישה חודשים לאחר הלידה, הפרעות בעצמות נצפות ונסוגות לא הייתה השפעה על התפרצות השיניים. עם זאת, ההשפעות על בלוטות הלימפה וההתאמה של השיניים נמשכו, ומינרליזציה קלה עד בינונית ברקמות שונות (של מתאם לא ברור עם הטיפול) נצפתה בבעלי חיים אחד. לפני הלידה לא נמצאו עדויות לנזק לאם; אירועים שליליים של האם לא דווחו במהלך הלידה. התפתחות בלוטת החלב של האם הייתה תקינה.
במחקרים באיכות עצם פרה-קלינית שנערכו בקופים שטופלו לטווח ארוך ב- denosumab, ירידה במחזור העצם לוותה בשיפור חוזק העצם והיסטולוגיה תקינה. רמות הסידן ירדו באופן זמני, בעוד שרמות ההורמונים הפאראתירואיד עלו באופן זמני אצל קופים שחולקו בשחלות שטופלו ב- denosumab.
בעכברים זכרים שעברו הנדסה גנטית לביטוי RANKL אנושי (עכברי נוקין) ועברו שבר טרנסקורטיקלי, דנוזומאב עיכב הסרת סחוס ושיפוץ יעלים בהשוואה לקבוצת הביקורת, אך החוזק הביו -מכני לא הושפע לרעה.
עכברי נוקאאוט (ראו סעיף 4.6) שלא הביעו RANK או RANKL הציגו ירידה במשקל, ירידה בצמיחת העצם וחוסר התפרצות שיניים. בחולדות בילודים, עיכוב של RANKL (מטרה של טיפול בדנוזומאב) עם מינונים גבוהים של אוסטאופרוטגרין המקושר ל- Fc (OPG-Fc) היה קשור לעיכוב של צמיחת עצם והתפרצות שיניים. במודל זה השינויים הללו היו הפיכים חלקית עם הפסקת הטיפול במעכבי RANKL. פרימטים בגיל ההתבגרות שטופלו במינונים של denosumab 27 ו -150 פעמים (מינונים 10 ו -50 מ"ג / ק"ג) גבוהים יותר מהמינונים המשמשים במרפאה הציגו חריגות. צלחות גדילה. לכן, טיפול ב- denosumab עלול לפגוע בצמיחת העצמות בילדים עם לוחות גדילה פתוחים ולמנוע את התפרצות השיניים.
06.0 מידע פרמצבטי
06.1 מרכיבים
חומצה אצטית קרחונית *
נתרן הידרוקסיד (להתאמת pH) *
סורביטול (E420)
פוליסורבט 20
מים להזרקות
* מאגר אצטט מתקבל על ידי ערבוב חומצה אצטית ונתרן הידרוקסיד
06.2 חוסר התאמה
בהיעדר מחקרי תאימות, אסור לערבב תרופה זו עם מוצרי תרופות אחרים.
06.3 תקופת תוקף
3 שנים.
ניתן לאחסן את פרוליה בטמפרטורת החדר (עד 25 מעלות צלזיוס) למשך עד 30 יום באריזה המקורית. לאחר הסרתו מהמקרר, יש להשתמש בפרוליה בתוך 30 יום זה.
06.4 אמצעי זהירות מיוחדים לאחסון
שומרים במקרר (2 ° C - 8 ° C).
אל תקפא.
שמור את המזרק הממולא בקרטון החיצוני כדי להגן על התרופה מפני אור.
06.5 אופי האריזה המיידית ותכולת האריזה
תמיסה של 1 מ"ל במזרק זכוכית חד פעמי למילוי חד פעמי עם מחט 27 מד נירוסטה, עם או בלי מגן מחט.
מכסה המחט של המזרק הממולא מכיל גומי טבעי יבש, שהוא נגזרת של לטקס (ראה סעיף 4.4).
גודל האריזה של מזרק אחד, עם שלפוחית (מזרק מלא עם או בלי מגן מחט) או ללא שלפוחית (מזרק מלא בלבד).
06.6 הוראות שימוש וטיפול
לפני הניהול יש לבדוק את הפתרון. אין להזריק את הפתרון אם הוא מכיל חלקיקים גלויים או אם הוא נראה עכור או לא צבוע. אין לנער יתר על המידה. כדי להימנע מתגובות באתר ההזרקה, אפשר למזרק הממולא להגיע לטמפרטורת החדר (עד 25 מעלות צלזיוס) לפני ההזרקה והזרק לאט. הזריק את כל תכולת המזרק הממולא. זרוק את כל שאריות התרופה שנותרו בתוך המזרק הממולא.
יש להיפטר מתרופות שאינן בשימוש ופסולת המופקת מתרופה זו בהתאם לתקנות המקומיות.
מחזיק רשות השיווק 07.0
Amgen Europe B.V.
מינרווום 7061
NL-4817 ZK ברדה
הולנד
08.0 מספר אישור השיווק
האיחוד האירופי/1/10/618/001
האיחוד האירופי/1/10/618/002
האיחוד האירופי/1/10/618/003
040108019
040108033
040108021
09.0 תאריך האישור הראשון או חידוש האישור
תאריך האישור הראשון: 26 במאי 2010
תאריך החידוש האחרון: 15 בינואר 2015
10.0 תאריך עיון הטקסט
יוני 2015








.jpg)